|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Página Principal | Universitario | Académico | Recursos | Tendencias | Laboratorios | Formularios | Glosario | Buscador |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
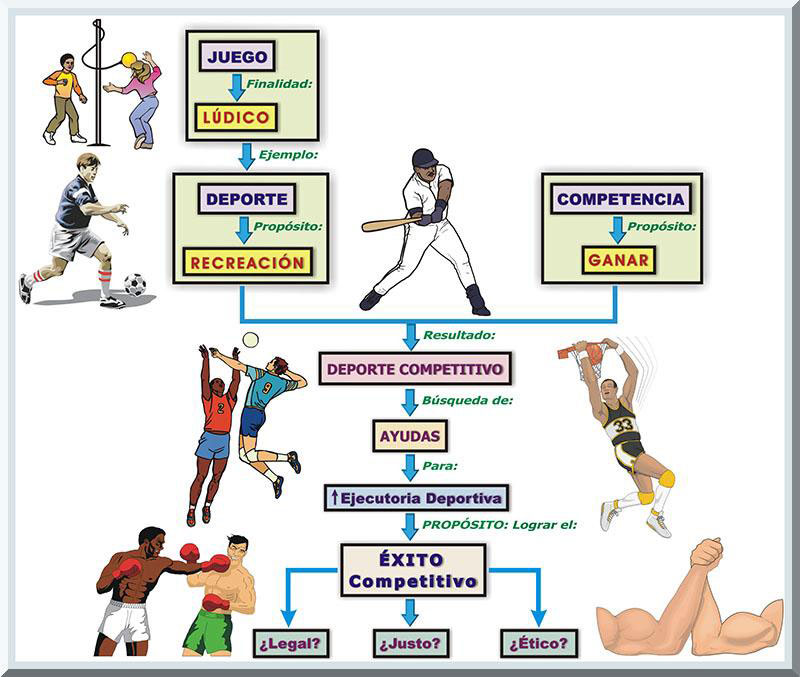
INTRODUCCIÓN Existe la disyuntiva entre el deporte y la competencia (véase Gráfico 1). La esencia del deporte es lúdica. No obstante, el enfoque competitivo puede transgredir la naturaleza festiva del deporte. Esto puede conllevar al uso de ayudas externas que asisten a la ejecutoria competitiva. De ninguna manera esto no significa que tales manipulaciones no sean éticas o se consideren ilegales. El problema consiste cuando se empleen protocolos que, posiblemente, mejoren el rendimiento atlético, pero se ubican en una posición desleal frente al adversario. La complicación principal ocurre cuando tales actividades sean prohibidas durante los eventos competitivos y posean efectos morfofuncionales hostiles a la salud del atleta (Eugenio, 2012).
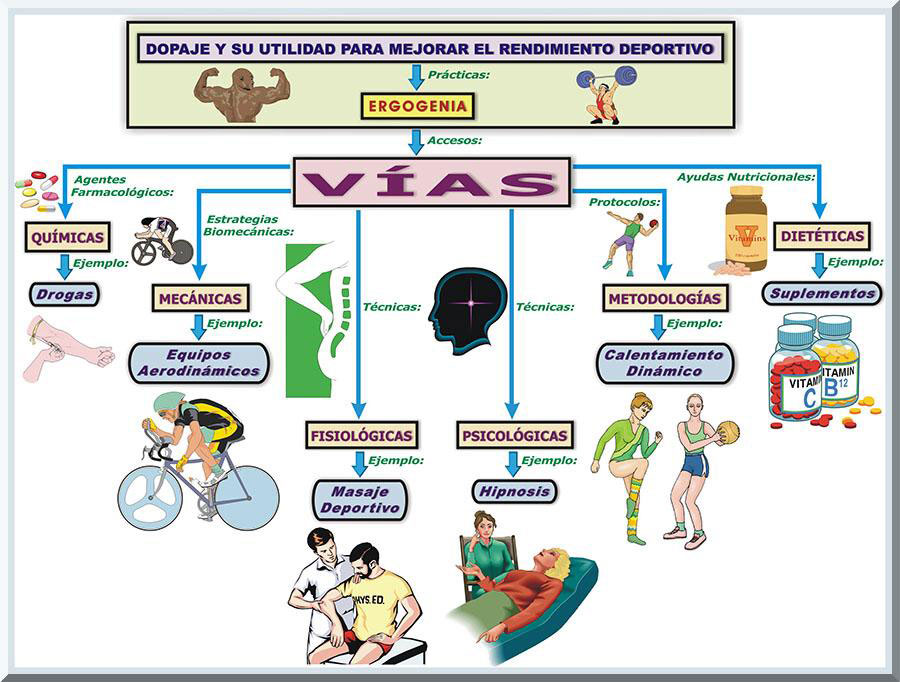
Los tipos de prácticas, o vías, comunes que potenciamente conduzcan a una mejor capacidad competitiva, se pueden clasificar en cinco categorías, que son: 1) químicas (Ej: drogas), 2) nutricionales (Ej: consumo de suplementos dietéticos), 3) biomecánicas (Ej: bicicletas fabricadas con ventajas aerodinámicas), 4) fisiológicas (Ej: masaje terapéutico), 5) metodológicas (Ej: incorporación del calentamiento previo a una sesión de ejercicio o competencia), y 6) psicológicas (Ej: técnicas de relajamiento mental) (Eugenio, 2012; Williams, 1998, p. 11) (véase Gráfico 2).
El uso inapropiado y desmedido de estos protocolos se puede considerar como una problemática desde el punto de vista ético o como un comportamiento ilegal (Eugenio, 2012). Entonces, no solamente la salud se considera como la única variable afectada por estos actos, sino también la responsabilidad del deportista de competir en igualdad de condiciones con su adversario. Sin embargo, desde la misma concepción del deporte, los competidores han incurrido en tales rutinas. No fue hasta las Olimpiadas de 1968 en México, donde se tomaron medidas para controlar y detectar el consumo se sustancias y el uso artificios para ayudar a los deportistas en su afán por obtener la preciada dorada (García-Arjona & Bodin, 2011). Desde entonces, el Comité Olímpico Internacional (COI), ha tomado el liderato en este asunto, estableciendo los controles y dictando el listado de fármacos y manipulaciones que se encuentran prohibidos en las competencias a nivel Olímpico. El COI posee varias alianzas internacionales, de las cuales una de las más relevantes es la Agencia Mundial Antidopaje (AMA). Tal organización internacional fue concebida en el año 1999 con el fin de controlar el dopaje en el ámbito del deporte competitivo (véase Gráfico 3).
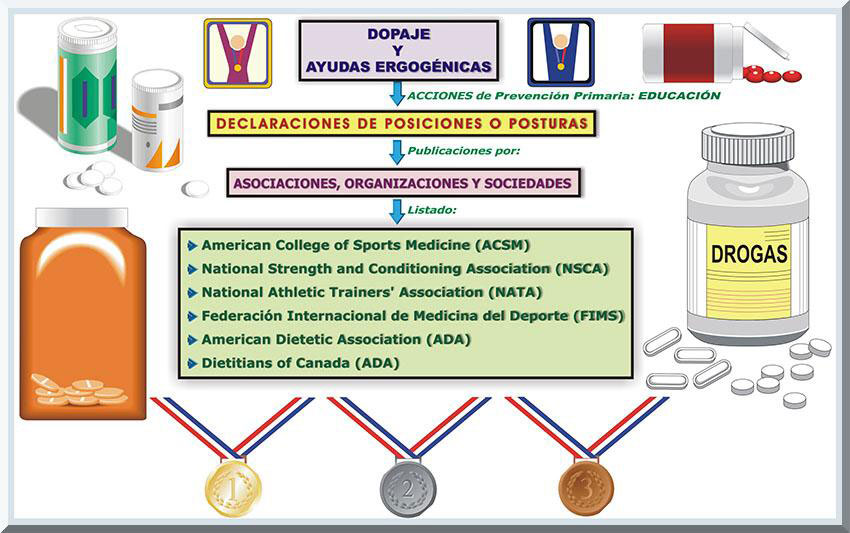
Además, ciertas asociaciones y sociedades, vinculadas con las ciencias del movimiento humano y la medicina del deporte, han publicado su postura ante el uso de las sustancias ergogénicas más comunes. Por ejemplo, la American College of Sports Medicine (ACSM), conjuntamente con la American Dietetic Association (ADA) y Dietitians of Canada (DC), han publicado una declaración de posición con respecto a la nutrición y el rendimiento deportivo, en la cual se incluye una sección que atañe a la ayudas ergogénicas (ACSM, ADA & DC, 2009). Además, la ACSM posee un documento donde indica su posición ante los esteroides anabolizantes-androgénicos (EAAs)(ACSM, 1987) y otro de dopaje sanguíneo (Sawka, Joyner, Miles, Robertson, Spriet & Young, 1996). Más recientemente, una declaración de postura similar fue expuesta por la National Athletic Trainers’ Association (NATA) (NATA, 2012). Por el otro lado, la National Strength and Conditioning Association (NSCA) ha expuesto su posición ante el uso de las sutancias anabólicas y la hormona de crecimiento entre la población atlética (Hoffman, Kraemer, Bhasin, Storer, Ratamess, Haff, Willoughby, & Rogol, 2009). Además, esta oganización ha publicado un boletín especial sobre tópicos vinculados con el uso y abuso de los esteroides anabólicos (NSCA, 2006). También, se han expresado diversas federaciones vinculadas con la medicina del deporte en el renglón internacional y latina, como lo son la Federación Internacional de Medicina del Deporte (FIMS) (FIMS, s.f.) y la Federación Española de Medicina del Deporte (FEMEDE) (FEMEDE, s.f.) (véase Gráfico 4). Además, ciertas organizaciones deportivas han enunciado su punto de vista concerniente al consumo de estos fármacos de naturaleza anabólicos y androgénicos, así como para el uso de drogas en las actividades atléticas. Algunas de tales entidades son la International Association of Athletics Federations (IAAF) (IAAF, s.f.), la National Federation of State High School Associations (NFHS) (NFHS, 2012), la South African Institute of Drug Free Sport (SAIDS) (SAIDS, 2011) y otras.
Una problemática de considerable magnitud es que una porción significativa de estos productos se pueden adquirir sin el requisito de una autorización médica. Por ejemplo, es posible que los atletas obtengan estas reclamadas ayudas químicas en gimnasios, tiendas de nutrición, farmacias y mediante los comercios electrónicos disponibles en la Internet/Web. TERMINOLOGÍA FUNDAMENTAL Con el objetivo de comprehender más efectivamente la teoría científica discutida en este documento, es vital describir conceptos comunes y esenciales expresados a través de la literatura que corresponde a los procedimientos empleados para mejorar la ejecutoria de los deportistas. CONCEPTOS BÁSICOS En primera instancia, es necesario entender que la ergogenia implica aquellos procedimientos, o sustancias, que pueden utilizar los atletas (o personas bajo un regimen de entrenamiento fisico) con miras de ayudarlos a incrementar la calidad de su ejecutoria competitiva. Literalmente, ergogenia significa producción de trabajo (del griego, ergon implica trabajo, mientras gennan significa producción) (Eugenio, 2012). Se considera que tal asistencia al competidor puede ser en la forma de sustancias farmacológicas, manipulaciones hematológicas e histoquímicas, nutrientes particulares (suplementos), aplicaciones de estrategias psicológicas, metodologías de calentamiento previo a una sesión de entrenamiento, empleo de artefactos mecánicos y otros. Se espera, entonces, que un producto reclamado como ergogénico mejore la capacidad del organismo humano en cuanto a la ejecutoria de diversas destrezas motrices particulares y en el rendimiento de los eventos de naturaleza competitiva (véase Gráfico 5). Lo correcto es que el deportista utilice ayudas ergogénicas que se consideren apropiadas (desde el punto de vista ético y legal) y no afecten el bienestar de éste. Estos tipos de protocolos incluyen una nutrición óptima durante el entrenamiento y competencia deportiva; el uso de suplementos dietéticos, según sea indicado a raíz de las necesidades individuales de cada competidor; el diseño de un programa de entrenamiento deportivo periodizado efectivo; la planificación triunfante de un entrenamiento deportivo de naturalza técnico-estratégico; el empleo de un calentamiento funcional durante las sesiones de entrenamiento físico y; la implementación exitosa de un entrenamiento mental para el deportista.
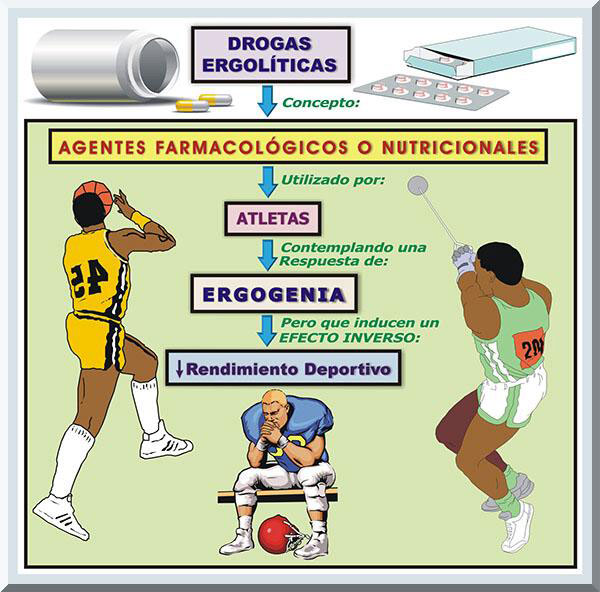
No todos los propuestos productos ergogénicos realmente ayudan al desempeño atlético, e inclusive, muchos de éstos resultan en efectos adversos a la salud del competidor. Esto es particularmente cierto cuando el deportista consume ciertas drogas, o suplementos dietéticos, que son reclamadas como ergogénicas, pero en la realidad el efecto es el inverso, es decir, se perjudica la ejecutoria competitiva del atleta. Bajo estas circunstancias, se considera a tal producto como una sustancia ergolítica (Eichner, 1989,1993). Consecuentemente, el uso de un grupo específico de fármacos, o sustancias nutricionales, que inducen un rendimiento deportivo desfavorable se denominan como elementos de naturaleza ergolítica, o simplemente, drogas ergolíticas (véase Gráfico 6). Por ejemplo, se ha evidenciado que las bebidas energéticas disminuyen la aptitud cardiorrespiratoria, de manera que tales prácticas son de naturaleza ergolítica, pues damnifican la ejecutoria del competidor (Sillivent, Blevins, & Peak, 2012).
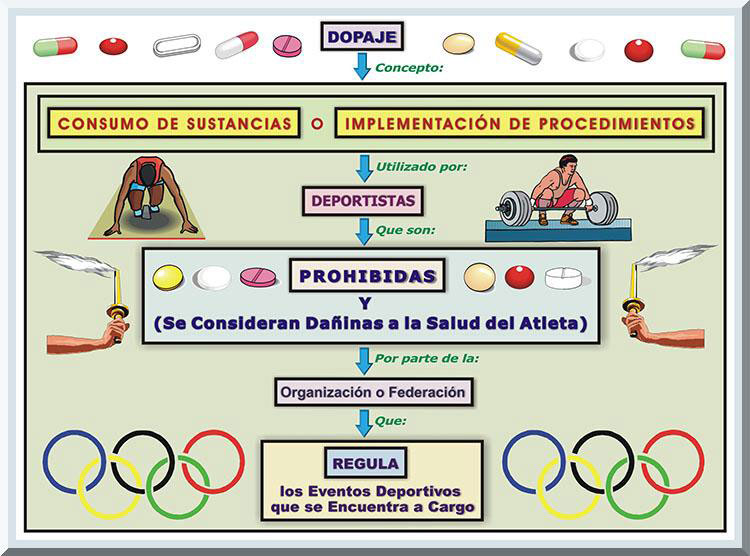
En ocasiones, algunos atletas se auto-administran ciertas sustancias en su organismo, o implementa un método específico, que son considerados ilegales, o prohibidos, por parte de algún tipo de organización, o federación, encargada de regular ciertos eventos deportivos particulares. Estos artilugios, que pueden ser perjudiciales para la salud del deportista, es conceptualizado como dopaje. Por consiguiente, se considera un procedimiento de dopaje cuando el competidor consume elementos ergogénicos, o realiza ciertos métodos, que se encuentran vedados por la entidad que organiza y rige las competencias deportivas (Fields & Turner, 2009; Müller, 2010) (véase Gráfico 7).
Como sabemos, una de las organizaciones de mayor renombre es el COI, la cual cuenta con un reglamento antidopaje. Este documento se halla la página Web oficial del COI (International Olympic Committee [IOC], 2012). Por su parte, la AMA, ha publicado el listado de sustancias prohibidas para las competencias olímpicas (Agencia Mundial Antidopaje [AMA], 2012) (véase Tabla 1). Además, esta colectividad ha desarrollado su propio reglamento de dopaje, conocido como el Código Mundial de Antidopaje (AMA, 2009).
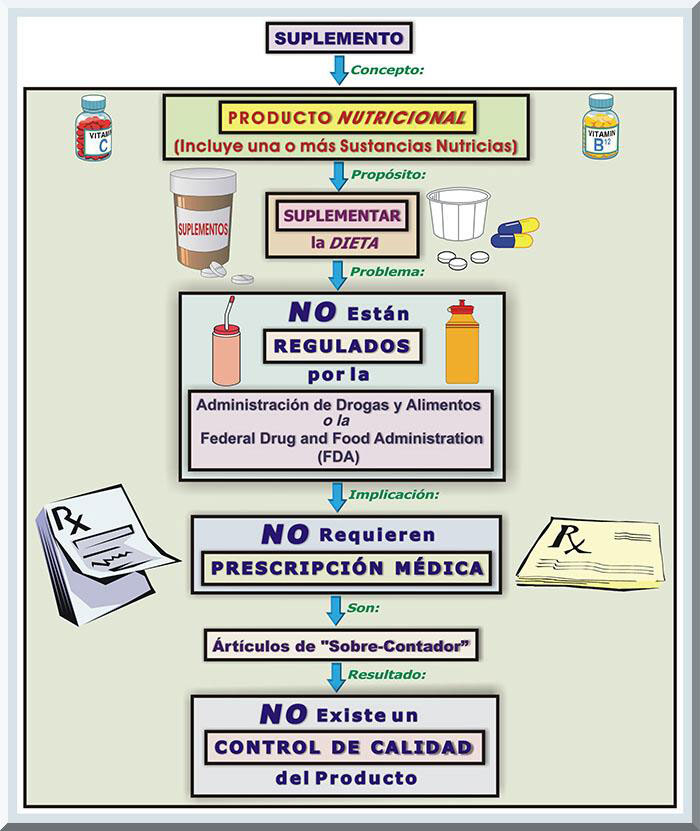
En los Estados Unidos Continentales, el gobierno federal ha establecido que un suplemento se clasifique como un producto, sin incluir los artículos relacionados con el tabaco, dirigido a suplementar la dieta. Según esta agencia federal, éstos elementos, de naturaleza dietética, incorporan uno o más sustancias nutricias, que son: aminoácidos, sustancias botánicas (Ej: hierbas o plantas), vitaminas, minerales o una mezcla de tales químicos (Fields & Turner, 2009). Entonces, aquellas sustancias que se no encuentren reguladas por la Administración de Drogas y Alimentos (FDA, siglas en ingles) son clasificadas como suplementos. Esto significa que los atletas, o competidores recreacionales, pueden comprar sin prescripción médica los productos considerados como suplementos. Consecuentemente, estos artículos de "sobre-contador" no cuentan con una auditoría estricta con respecto al control de calidad de los elementos químicos que constituyen tales suplementos. El deportista, pues, puede creer que ha obtenido un producto de alta calidad, cuando en realidad este no es el caso real (véase Gráfico 8).
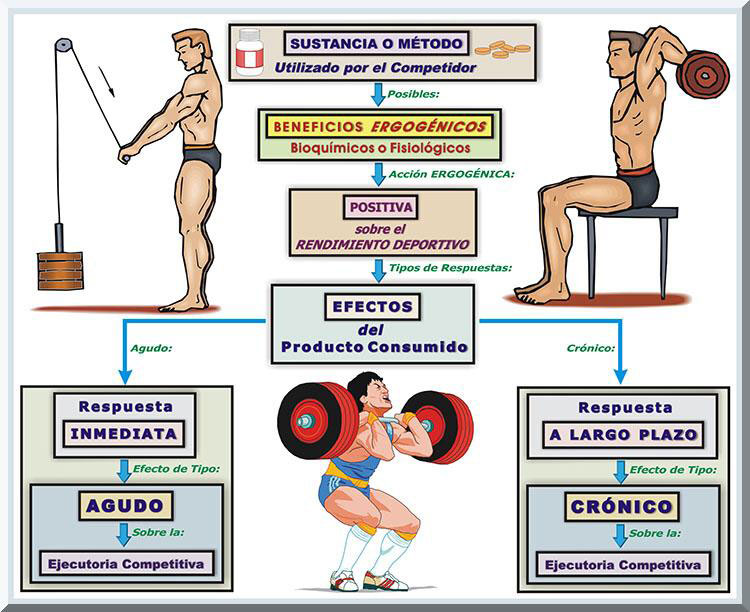
Los posibles beneficios bioquímicos o psicológicos de aquellas sustancias, o métodos, que pueden afectar positivamente el rendimiento deportivo se clasifican como efectos agudos o crónicos. Cuando las ayudas ergogénicas inducen cambios fisiológicos o psicológicos inmediatamente después de su utilización se dice que tal asistencia posee un efecto agudo sobre la ejecutoria deportiva. Por el contrario, se evidencia un efecto crónico sobre la capacidad deportiva del atleta cuando tal elemento ergogénico se requiere emplear a lo largo de un periodo particular durante el entrenamiento deportivo del atleta (Titchennal, 2010) (véase Gráfico 9).
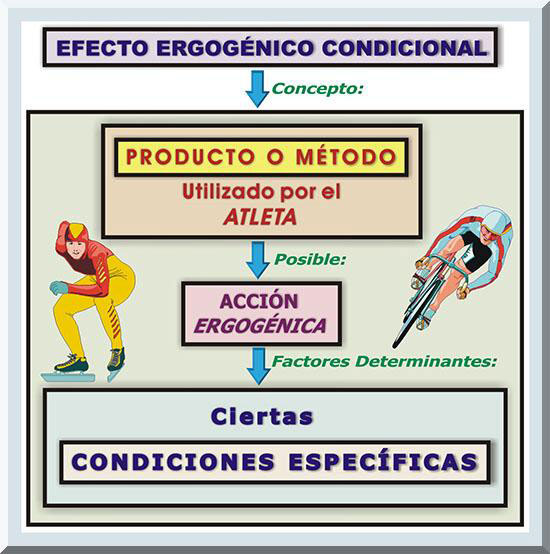
En ocasiones, los efectos benéficos de la ayuda ergogénica dependerán de ciertas condiciones específicas. Esto se conoce como un efecto ergogénico condicional (Titchennal, 2010) (véase Gráfico 10).
PROBLEMAS DE DISEÑOS
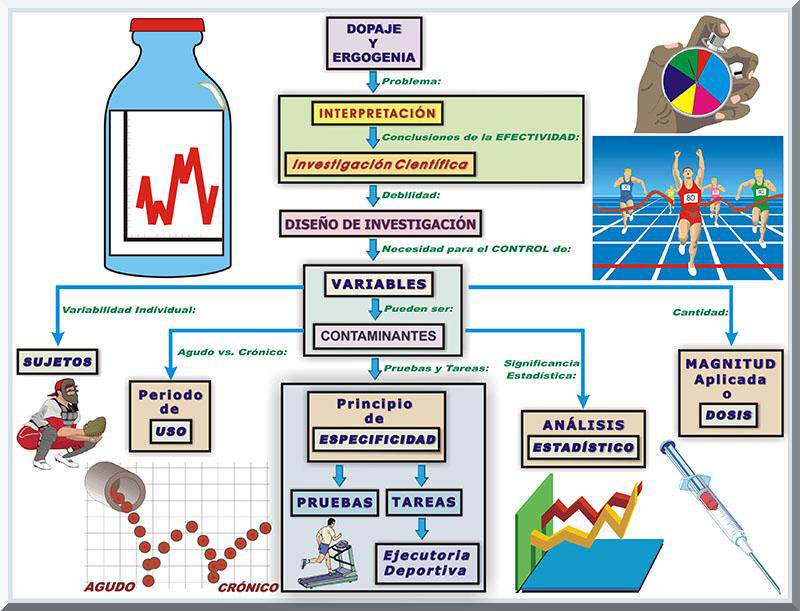
EXPERIMENTALES El diseño experimental de algunas investigaciones científicas que han estudiado la efectividad del uso de una gama amplia de ayudas ergogénicas, pueden estar viciados por un pobre control de las variables independientes, o contaminado por otras variables que bien pudieran haber alterar los hallazgos del estudio. Estos factores pueden agruprase en cinco categorías principales, que son: 1) sujetos (Ej: variabilidad individual), 2) periodo de uso (Ej: efecto agudo versus crónico), 3) principio de especificidad (para las pruebas de laboratorio y los tipos de tareas atléticas particulares), 4) cantidad o dosis, y 5) significancia estadística (Kraemer, Fleck & Deschenes, 2012, p. 416; Powers & Howley, 2007, p. 523) (véase Gráfico 10).
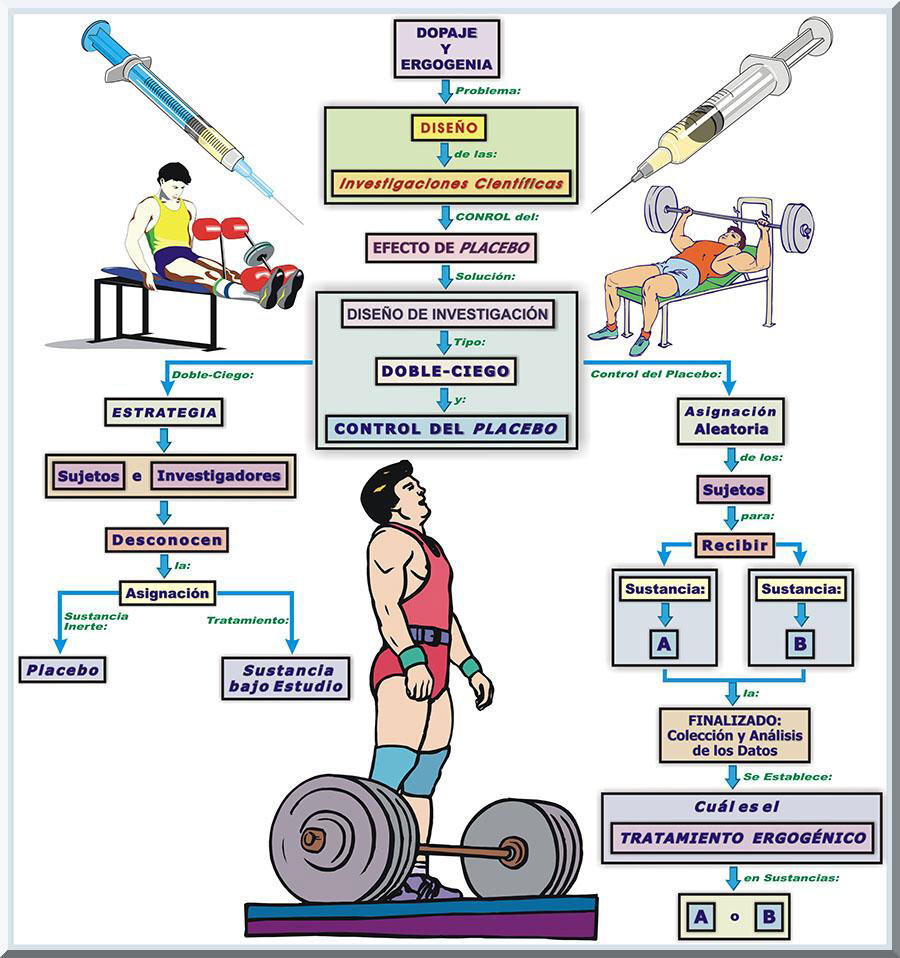
Un ejemplo clásico de un pobre diseño experimental es no poder controlar los efectos subjetivos, o psicológicos, de las sustancias que consumen los deportistas durante la investigación. Comúnmente, este fenómeno se conoce como el efecto de placebo. Entonces, para controlar tal tipo de fenómeno, será necesario incluir, en el diseño del estudio, la administración de un placebo a un grupo de sujetos, seleccionados aleatoriamente. Un placebo es, pues, una sustancia similar al agente ergogénico bajo investigación, pero no ejerce ningun efecto fisiológico. También, es posible que los investigadores, inconscientemente, se prejuicien tocante al efecto positivo de la ayuda ergogénica estudiada, es decir, éstos pueden estar confabulados en la creencia de que, en efecto, existe un efecto de ergogenia en el producto estudiado. Para resolver tales debilidades, es imperante establecer un diseño de investigación doble-ciego. En tal modelo experimental, ni los investigadores, ni los sujetos, conocen quienes están recibiendo el tipo de ayuda ergogénica y a qué grupo de sujetos se le administran el placebo. Esto significa que, en este modelo, se le asigna aleatoriamente, a la muestra poblacional, una sustancia A y B. Entonces, una vez finalizado el proceso de colectar los datos de la investigación, así como la aplicación de su correspondiente tratamiento estadístico, se releva cuál de las dos sustancias (A o B) es la que incluye el tratamiento ergogénico (véase Gráfico 12).
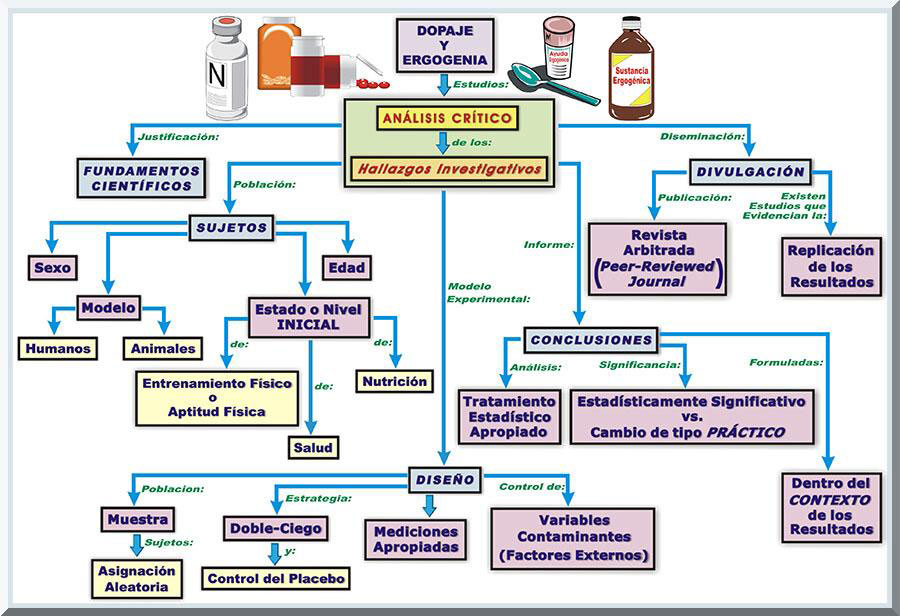
PROBLEMÁTICA DEL CONTROL EXPERIMENTAL Todo tipo de estudio experimental se encuentra sujeto a diversas problemáticas de diseño, lo cual pueden afectar la variable independiente, es decir, la alegada ayuda ergogénica de algún agente en específico. Tales alteraciones de validez y confiabilidad, por parte de los hallazgos y conclusiones, pueden surgir de un conjunto de factores, que son: 1) selección de una muestra poblacional no aleatoria; 2) ausencia de un diseño experimental de tipo doble ciego; 3) pobre control del efecto de placebo; 4) presencia de errores que se incurren durante las mediciones experimentales; 5) diferencias individuales entre los participantes; 6 ) diversidad individual de los cambios circardiados cotidianos con respecto a las respuestas del supuesto elemento ergogénico; 7) deficiente control en otras variables (dependientes) de tipo contaminantes; 8) inhabilidad por parte de los investigadores de considerar los efectos que poseen de la edad y sexo sobre la variable independiente; 9) inconsistencia en el contexto experimental donde se realizan las evaluaciones de la ejecutoria deportiva (especificidad de la prueba); 10) variabilidad tocante al tipo de ejecutoria atlética evaluada (especificidad de la tarea deportiva); 11) condiciones ambientales variables (Ej: temperatura, humedad, contaminación ambiental) bajo las cuales se llevan a cabo las pruebas experimentales; 12) fallo de un control en cuanto a la cuantificación de la dosis administrada del agente ergogénico; 13) falta de un establecimiento del estado de nutrición de los sujetos previo ha ser sometidos al protocolo experimental; 14) tratamiento estadístico inapropiado y poco práctico (Ej: no limitarse úticamente al nivel de significancia estadística para llegar a conclusiones); 15) carencia de realizar el correspondiente análisis del nivel de entrenamiento en que se encuentran los sujetos; 16) en estudios con animales, generalización a seres humanos fundamentado en los hallazgos de varios géneros de animales; 17) consideraciones en cuanto a los efectos agudos versus crónicos del propuesto elemento ergogénico; 18) planteamientos de conclusiones más allá de los resultados obtenidos en la investigación científica; 19) informe del estudio investigativo publicado en una revista no profesional, donde no se requiere una evaluación rigurosa por parte de otros colegas del campo; 20) incapacidad de poder reproducir la investigación científica; y otras (Kenney, Wilmore & Costill, 2012, p. 399; Kraemer, Fleck & Deschenes, 2012, p. 416; McArdle, Katch, & Katch, 2010, pp. 538-540). En resumen, durante el proceso de analizar críticamente los informes de las diversas investigaciones científicas que estudian la efectividad de algun agente egogénico en particular, es imperante considerar diversos factores, que son, a saber: 1) la justificación del trabajo (i.e., su fundamento científico); 2) la población o sujetos (edad, sexo, humanos vs. animales, nivel inicial de entrenamiento físico o aptitud físca, estado base del bienestar de los participantes y el estado nutricional de comienzo de tales sujetos); 3) el tipo diseño experimental (Ej: doble-ciego y control del placebo, estrategia establecida evitar la influencia de variables contaminantes, selección aleatoria de la muestra y uso apropiada de las mediciones); 4) la formulación de las conclusiones (se realizan dentro del contexto de los resultados, se considera la significancia estadística y la práctica, se utiliza el tratamiento estadístico adecuado de los datos); y 5) la diseminación del estudio (publicado en una revista arbitrada [peer-reviewed journal] y los hallazgos de la presente investigación han sido replicados en otro estudio) (McArdle, Katch, & Katch, 2013, pp. 353-354; McArdle, Katch, & Katch, 2010, pp. 538-540) (véase Gráfico 13).
POSIBLES MECANISMOS MEDIANTE
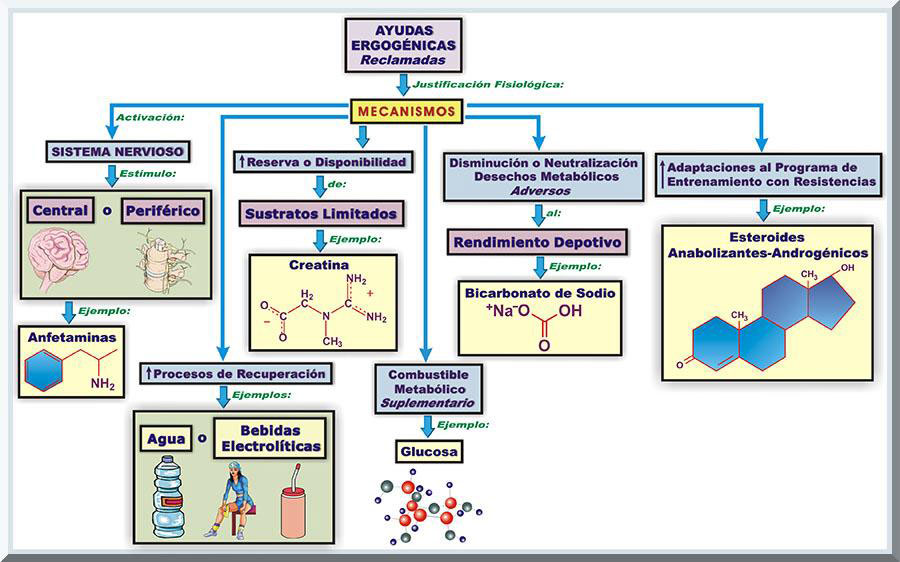
LOS CUALES TRABAJAN La justificación fisiológica para las sustancias, o artefactos, que probablemente promuevan una ejecutoria competitiva exitosa se ha documentado en la literatura científica (McArdle, Katch & Katch, 2010, p. 541). En los próximos párrafos se discutirán tales ventajas propuestas por parte de los productos ergogénicos (véase Gráfico 14).
ACTIVACIÓN DEL SISTEMA NERVIOSO Se ha señalado que un colectivo particular de agentes ergogénicos se encargan de proveer un estimulo adecuado al sistema nervioso, tanto a su componente central como el periférico. Algunos de estos fármacos, que se utilizan por la virtud que pueden inducir tales respuestas, son las anfetaminas, cafeína, alcohol, colina y otros. INCREMNTO EN LA PROVISIÓN O ALMACENATO DE COMPUESTOS QUE POSIBLEMENTE PROMUEVAN LA TRANSFERENCIA ENERGÉTICA O POSEAN UN ESTÍMULO DE NATUTALEZA ANABÓLICO Otro propuesto medio por el cual se experimenta el fenómeno de la ergogenia consiste en una mayor disponibilidad, o reserva, de ciertos sustratos que comúnmente no abundan en el organismo humano. Se propone, pues, que tales compuestos asisten al rendimiento atlético efectivo. Como constituyentes de este grupo, podemos mencionar a la carnitina, creatina, el cromio, los hidratos de carbono y otros productos de acción similar. COMBUSTIBLE METABÓLICO ALTERNO Se ha sugerido que otro colectivo de elementos contribuye a una mejor ejecutoria deportiva al servir como un suplemento bioenergético esencial. Entonces, tales moléculas son responsables de disponer un fácil acceso de energía para los tejidos que así lo requieran (Ej: músculos esqueléticos). Entre estas sustancias encontramos a la glucosa, triglicéridos de cadena mediana, entre otros semejantes. BLOQUEO DE COMPUESTOS BIOQUÍMICOS QUE AFECTAN ADVERSAMENTE LA EJECUTORIA COMPETITIVA Ciertos productos, de supuesta naturaleza ergogénica, se engargan de neutralizar o inhibir los desechos metabólicos que perjudican a la ejecutoria deportiva. Bajo esta categoría, podemos mencionar al bicarbonato de sodio (o citrato de sodio), el fosfato, ácido pangámico (o vitamina B12) y otros. PROCESOS DE RECUPERACIÓN EFICASES Algunas sustancias nutricias promueven una mejor, y rápida, recuperación durante, y luego, de un ejercicio agudo, incluyendo el periodo posterior a una competencia deportiva. Entre estos compuestos, encontramos aquellos hidratos de carbono que poseen un alto índice glucémico, agua, bebidas electrolíticas y otros. MAYOR EFECTIVIDAD ANTE LAS ADAPTACIONES QUE RESULTAN DE UN PROGRAMA DE ENTRENAMIENTO CON RESISTENCIAS Finalmente, existen varios productos que mejoran la calidad de las adaptaciones a un sistema de entrenamiento deportivo dirigido al desarrollo de la aptitud muscular. Por lo regular, las sustancias que inducen tal efecto son los EAAs, la hormona de crecimiento humano (growth hormone o GH, siglas en ingles), y diversos suplementos dietéticos en la forma de hidratos de carbono y proteinas consumidos inmediatamente luego del ejercicio. USO Y ABUSO DE DROGAS, Las ansias psicopatológicas de aquellos atletas que solo se concentran en lograr la victoria a través de cualquier medio posible, sin tener en consideración el competir de manera "limpia", conducen a este deportista a la farmacodependencia de sustancias que podrían ser mortales a largo plazo. Al presente, las siete sustancias farmacológicas prohibidas, según la AMA (AMA, 2012), en competencias internacionales son, a saber: 1) esteroides anabolizantes androgénicos, 2) hormonas pépticas y otras sustancias relacionadas, 3) agonistas beta-2, 4) moduladores hormonales y metabólicos, 5) diuréticos y otros agentes enmascaran los sustancias consumidas, 6) estimulantes, 7) narcóticos, 8) canabinoides, y 9) glucocorticoesteroides. Además, se prohíben ciertos métodos de dopaje, como lo son: 1) el aumento en la transferencia de oxígeno (Ej: dopaje sanguíneo), 2) manipulación química y física de las muestra de dopaje, y 3) el dopaje genético. Finalmente, existen algunas sustancias que están prohibidas solo en ciertos deportes que son: 1) el alcohol, y 2) betabloqueantes (véase Tabla 1).
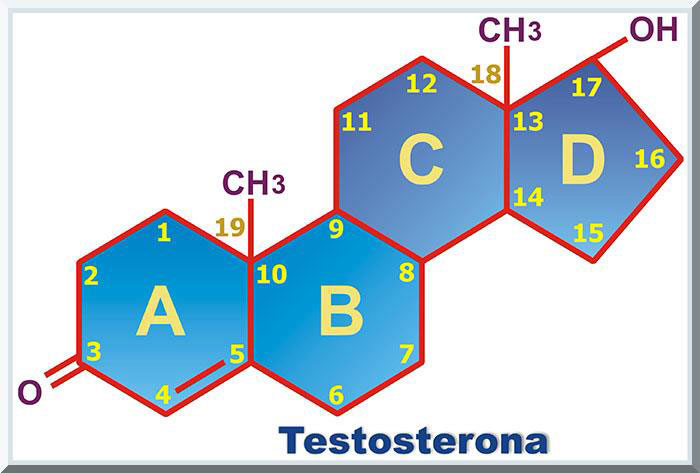
ESTEROIDES ANABOLIZANTES Y ANDROGÉNICOS Este grupo de agentes farmacológicos de naturaleza anabólica se ubican en el listado prohido por parte de varias organizaciones deportivas. Entre tales entidades, encontramos al COI, la Fédération Internationale' de Football Association (FIFA), la National Collegiate Athletic Association (NCAA), el Mayor League Baseball (MLB), la National Basketball Association (NBA), la National Football League (NFL), y otras (Juhn, 2003). Los esteroides, como lo son la testosterona y su metabolito dihidrotestosterona, poseen dos tipos de acciones integradas. La primera es de tipo androgénico, o virilizante (masculinizante), evidenciado por la manifestación de los caracteres sexuales secundarios durante la maduración del adolescente varón en su etapa de pubertad, como lo son: 1) crecimiento piloso corporal (Ej: facial, axilar y púbico); 2) desarrollo sistema reproductorio (Ej: escroto, testículos, pene, próstata, vesículas seminales y epidídimo); 3) agrandamiento de la laringe y engrosamiento de las cuerdas vocales (ocasionando una voz más grave o ronca), entre otros cambios (Griffin & Wilson, 1989). En el otro extremo, la testosterona cuenta con una función de tipo anabólica (i.e, de síntesis). Este tipo de acción: 1) estimula el desarrollo de la masa muscular y tejido conectivo (como resultado de una mayor retención de nitrógeno); 2) incrementa el tejido óseo; 3) aumenta el proceso de la hematopoyesis (esto induce a un aumento en el hematocrito); y 4) se evidencia una aceleración del crecimiento lineal (la talla) y aumento de la masa corporal (MC) (Griffin & Wilson, 1989; Manso, 1992; Underwood & Van Wyk, 1989). Entonces, podemos llamar a estas drogas como esteroides anabolizantes-androgénicos (EAAs).
ESTEROIDES ANABOLIZANTES Y ANDROGÉNICOS Aquellos esteroides anabolizantes y androgénicos que provienen del sistema endocrino natural que secreta el organismo humano, se conocen con el nombre de EAAs endógenos. Por su parte, los EAAs exógenos se derivan de productros químicos generados por las farmaceúticas, es decir, son elaborados de manera sintética.
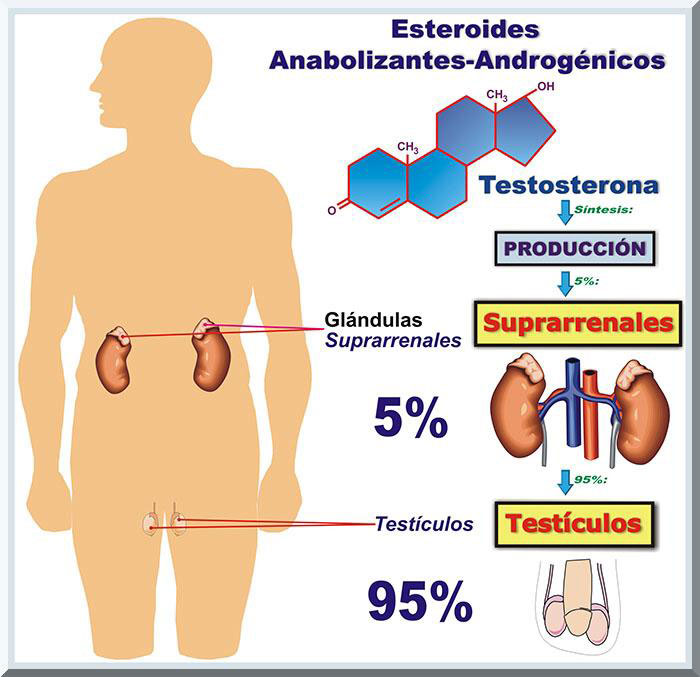
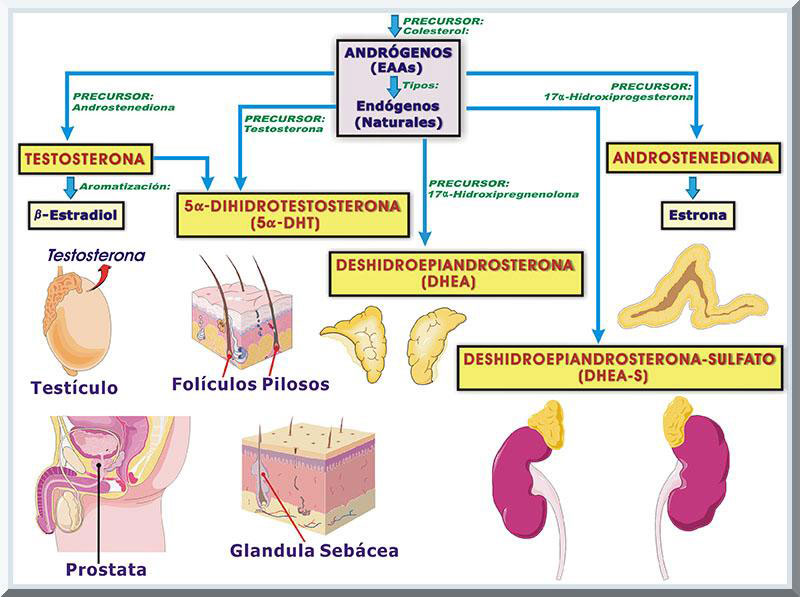
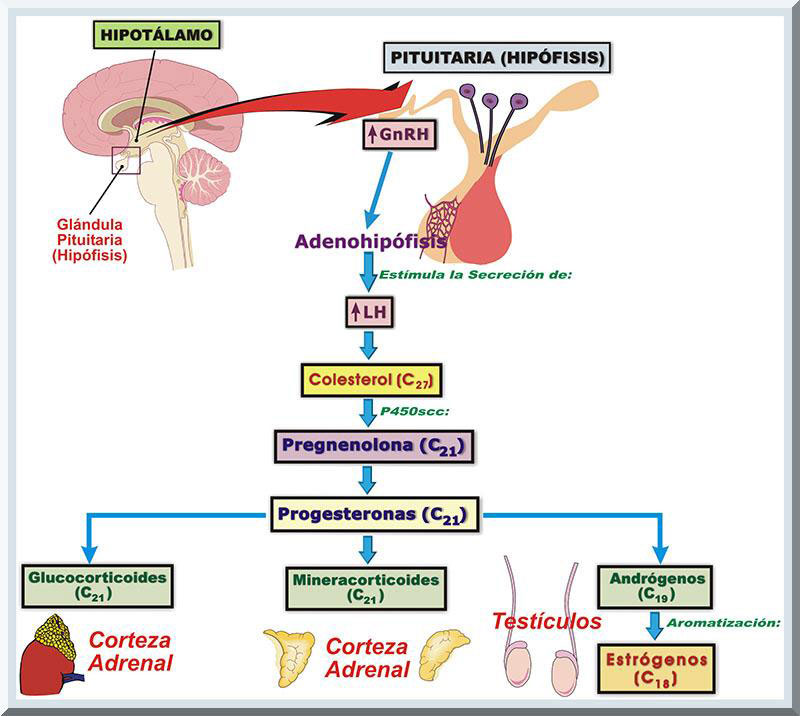
Farmacocinética El grupo de EAAs que se obtienen sintéticamente, son derivados de la testosterona natural (véase Gráfico 15), cuyas concentraciones séricas son mayores en la población masculina. Este tipo de esteroide lo sintetizan, principalmente, las gónadas. Gran parte (95%) de los EAAs naturales se produce principlamnete en las gónadas de los varones (i.e., células de Leydig en los testículos) (McArdle, Katch, & Katch, 2010, p. 541). El cinco por ciento de la testosterona secretada en el organismo humano proviene de las glándulas suprarrenales (véase Gráfico 16). En adultos varones, la producción testicular de la testosterona flutúa desde 2.5 a 11 miligramos (mg) por día (Wadler & Hainline, 1989, p. 58). En la población envejeciente, disminuye la concentracion sérica de testosterona, lo cual genera ciertos cambios biológicos que son evidentes en edades avanzadas. Algunos de tales alteraciones morfofuncionales evidentes en el varon envejeciente con sarcopenia (reducción en la mass musculesqulética), disminución en la fortaleza muscular, menor densidad ósea, menor libido y reducción en la disponibilidad energética. El restante de las sustancias androgénicas naturales son los andrógenos adrenales (secretasos por la corteza adrenal), que son, androstenediona, deshidroepiandrosterona (DHEA) y DHEA-sulfato (DHEA-S), y el metabolito de la testosterona 5α-dihidrotestosterona (5α-DHT) (Cantabrana, Hidalgo & Sánchez, 2009; Kicman, 2010; Swaminathan, 2011, p. 529). Los andrógenos adrenales (DHEA, DHEA-S y androstenediona) pueden ser transformados en testosterona y dihidrotestosterona en el hígado y tejidos diana (periferales), tales como el folículo piloso, las glándulas sebáceas, la próstata y genitales externos (Cantabrana, Hidalgo & Sánchez, 2009; Swaminathan, 2011, p. 529) (véase Gráfico 17). Se ha evidenciado que el efecto farmacológico de los EAAs solo se obtiene por medio de la alteración química de los andrógenos naturales (Ej: la testosterona). Esto responde al hecho que la testosterona administrada de forma oral se inactiva a través del metabolismo hepático, desde donde se transforma en androsterona y etiocolanolona (metabolitos inactivos), y en 5α-DHT y estradiol (metabolitos activos) (Cantabrana & Sánchez, 2009; Wadler & Hainline, 1989, p.60; Brunton, Parker, Blumenthal & Buxton, 2008, p. 1012) (véase Gráfico 18). Consecuentemente, se han desarrolado varios métodos bioquímicos para la producción de EAAs exógenos más efectivos, entre los cuales se encuentran: 1) la esterificación en posición 17ß del grupo hidroxil con los ácidos carboxílicos y 2) el alquilado en posición 17α (Brunton, Parker, Blumenthal & Buxton, 2008, p. 1017; Cantabrana & Sánchez, 2009; Wadler & Hainline, 1989, p.60). Al presente, en Estado Unidos Continentales, el Reino Unido y en Europa, existen varias compañías farmaceúticas que producen EAAs sintéticos. Entre los tipos de esteroides anabólicos que se administran vía oral, encontramos a: 1) estanozolor (Winstrol®, Stromba); 2) oximetolona (Anadrol 50®, Anapolon, Adroide); 3) metandrostenolona (Dianabol, Dialone); 4) metiltestosterona (Androide, Metandren, Arcosterone); 5) fluoximestrerona (Androide-F, Halostestin®, Ultrandren); 6) noretandrolona (Nilevar); 7) etilesterol (Maxibolin, Orabolin®); 8) testosterona undecanoata (Restandol, Andriol, Undestor, Pantestone), 9) metenolona (Primobolan®, Depot); y 10) mesterolona (Pro-Viron) (Kicman & Gower, 2003). Por el otro lado, los EAAs exógenos inyectables son, a saber: 1)estanozolor (Winstrol® V, Stromba); 2) nandrolona decanoata (Androlone-D 200, Deca-Durabolin®, Hybolin Decanoate, Nandrobolic LA); 3) nandrolona fenilpropionato (Anabolin, Androlone, Durabolin®); 4) drostanolona propionata (Droiban, Masteron, Masteril, Metormon, Permastril); 5) boldenona undeclinata (Equipoise®, Vebonol); 6) trenbolona acetato (Finajet, Finaplix-H®, Finaject); 7) testosterona propionata (Androlan, Testex, Leo, Vironmone); 8) testosterona propionata, fenilpropionata, isocaproata, decanoata (Sustanon); 9) testosterona cipionata (Andro-cyp, Andronaq LA, Andronate, Depotest, Depo-Testosterone); y 10) testosterona enantato (Andro LA 200, Andryl 200, Delatestryl, Primosteron®-Depot, Tesloviron®-Depot) (Graham, Davies, Grace, Kicman & Baker, 2008). Definición, Estructura Química La familia de los esteroides se caracterizan por poseer tres anillos compuestos de seis carbonos cada uno, desde el cual se enlaza un anillo constituido de cinco carbonos. El colesterol representa una estructura básica de este colectivo, de manera que es un precursor de todos los agentes que se derivan de tal estructura fundamental de los anillos (Berg, Tymoczko, Stryer & Gatto, 2012, p. 780; Garrett & Grisham, 2013, p. 248; Kishner, & Griffing, 2001). Entre los esteroides hormonales sintetizados del colesterol, encontramos a la progesterona, los glucocorticoides, mineralocorticoides, los andrógenos y estrógenos (Berg, Tymoczko, Stryer & Gatto, 2012, p. 780; Garrett & Grisham, 2013, p. 249). El estímulo para lo producción de los andrógenos se origina mediante la liberación de las hormonas sintentizadas en la adenohipófisis (lóbulo anterior de la hipófisis o pituitaria). Específicamente, se trata de las gonadotropinas, particularmente la homona luteinizante (LH), aunque su acción es más efectiva en la presencia de la Hormona Estimulante de Folículo (Follicle Stimulation Hormone o FSH, siglas en ingles). Durante la pubertad, estas hormonas son reguladas por la Hormona Liberadora de Gonadotropinas (Gonadotropin-Releasing Hormone o GnRH, siglas en ingles), las cuales son producidas a nivel de las células nerosecretoras del hipotálamo (Cantabrana & Sánchez, 2009) (véase Gráfico 19). Entonces, se establece que los esteroides anabolizantes representan una familia de compuestos químicos vinculados, estructural y funcionalmente, con los andrógenos, particularmente la hormona testosterona (Berg, Tymoczko, Stryer & Gatto, 2012, pp. 784-785; Graham, Davies, Grace, Kicman, & Baker, 2008; Haupt & Rovere, 1984; Manso, 1992).
Las concentraciones de la hormona androgénica (másculina) principal (i.e, testosterona) son de 20 a 30 veces más bajas en mujeres, al compararse con los varones (Kraemer, Fleck & Deschenes, 2012, p. 422). Este dato implica que, a pesar que el grupo femenino se someta a un programa de entrenamiento con resistencias, no se habrán de observar las marcadas adaptaciones de hipertrofia muscular que es común en los deportistas varones. Además, en aquellas circunstancias donde la población femenina atlética consuma EAAs exógenos (o sintéticos), no se observarán cambios dramáticos, de tipo anabólico en los músculos esqueléticos. Esto responde la reducida concentración basal (normal o de inicio) de andrógenos, en comparación con el colectivo varón. Consecuentemente, existe una alta probabilidad de que estas mujeres sufran de complicaciones de salud, pues podrían generar cambios androgénicos en diversos tejidos del cuerpo, los cuales son irreversibles (Kraemer, Fleck & Deschenes, 2012, p. 422). Tales alteraciones son las que experimentan los varones durante los inicios de la pubertad, es decir, las características sexuales secundarias de naturaleza masculinizante. Por ejemplo, algunos de estos cambios pueden ser, crecimiento de vello facial, voz con un tono más grave y otros (Rowland, 1996, pp. 9-10). Acciones Farmacológicas de los EAAs La mitad de las acciones farmacológicas de tipo androgénica, que disponen el colectivo de los EAAs, proviene de la testosterona. Por su parte, la androsterona y la deshidroepiandrosterona (DHEA) disponen de una contribución androgénica de 8% y 4%, espectivamente (Cantabrana, Hidalgo & Sánchez, 2009). La testosterona, que predomina en la población masculina, representa la hormona principal responsable en generar las características sexuales secundarias en el varón. Algunas de estas características incluyen las diferencias sexuales concerniente a la masa y fortaleza muscular, común durante el periodo de la pubertad. Estas acciones viriliznantes o masculinizantes (i.e., androgénicas) y anabolizantes ocurren simultanememte durante esta etapa de vida del varón. Además, en los tejidos periferales, la testosterona se transforma en dihidrotestosterona (DHT) por la acción de la 5α-reductasa (Berg, Tymoczko, Stryer & Gatto, 2012, p. 785; Kicman, 2010). A nivel del neonato, tal acción permite el desarrollo de estructuras reproductivas masculinas (Ej: los genitales externos, la próstata y vecículas seminales) . Más aún, la hormona DHT ejerce, predominantemente, ciertos efectos de tipo androgénicos a nivel del tejido integumentario (piel), la próstata y las glándulas accesorias que posee el varón (Casavant, Blake, Griffith, Yates & Copley, 2007). Sin embargo, existen, también, efectos de naturaleza estrogénica. Por ejemplo, los estrógenos promueven la osificación de las placas epifisarias de los huesos en crecimiento. Además, estas hormonas poseen una acción de carácter anabólico sobre el tejido óseo. También, la regulación homeostática del complejo enzimático P450 aromatasa (gen CYP19) se produce mediante la retrocomunicación negativa de la secreción de las gonadotropinas por parte del estímulo a nivel de hipotálamo (Cantabrana, Hidalgo & Sánchez, 2009). La acción de la aromatasa sobre la testosterona y androstenediona resulta en la producción de estradiol y estrona (un tipo de estrógeno), respectivamente (Berg, Tymoczko, Stryer & Gatto, 2012, p. 785). Este evento contribuye al 85% de la concentración sérica total del estrógeno que posee la población masculina (Brunton, Parker, Blumenthal & Buxton, 2008, p. 1012). Bajo aquellos casos en los cuales se administra una alta dosis de EAAs, la enzima aromatasa induce una elevada concentración de el estrógeno circulante (Hartgens & Kuipers, 2004). Indicaciones Médicas Existe una variedad de contextos clínicos que pueden estar indicados los esteroides de tipo anabólicos. Entonces, bajo supervisión médica, los EAAs sintéticos (exógenos) ofreceb una alternativa terapéutica ante las siguientes circunstancias: 1) patologías que que inducen un estado catabólico y pérdida de la masa musculoesquelética (Ej: síndrome de inmunodeficiencia adquirida o SIDA); 2) estados catabólicos, con evidencia de proteólisis, que resulta del tratamiento prolongado de costicosteroides; 3) envejecientes con evidencia de sarcopenia; 4) la presencia de neoplasmas malignos en el seno; 5) insuficiencia cardiaca; 6) osteoporosis; 7) hipogonadismo primario y secundario; 8) niños con deficiencia de testosterona cerca de la pubertad o retraso en su crecimiento ponderal; 9) diversos tipos de anemia (Ej: anemias hemolíticas y anemia de Fanconi); 10) ciertos disturbios hematológicos (Ej: púrpura trombocitopénica idiopática y mielofibrosis; 11) deficiencia de andrógenos en la población envejeciente; 12) estados caquécticos, donde se evidencia un consumo deficiente de calorías y proteínas (Ej: anorexia nervosa y bulimia); 13) quemaduras de tercer grado; 14) presencia de heridas agudas y crónicas; 15) contracepción masculina; 16) angioedema hereditario (disturbio de naturaleza genético caracterizado por la deficiencia de el inhibidor de C1 esterasa o C1-INH); y otras (Brunton, Parker, Blumenthal, & Buxton, 2008, pp. 1019-1021; Cantabrana, Hidalgo & Sánchez, 2009; Kishner & Griffing, 2011; Sari, 2010). La situación alarmante es que estos fármacos constantemente se están empleando por atletas que buscan inducir una rápida y marcada hipertrofia muscular. Entre los deportistas que consumen con frecuencia estas sustancias se encuentran los fisiculturistas, aquellos que practican halterofilia (levantamiento de peso olímpico), atletas de pista y campo (particularmente aquellos que demandan la producción de un elevada potencia y fortaleza muscular), jugadores de béisbol (comúnmente jugadores profesionales), jugadores profesionales de futbol Americano, ciclistas de carretera, entre otros. Según se habrá de discutir más adelante en el presente documento, este uso desmedido puede resultar en graves problemas clínicos. Efectos Morfofuncionales Propuestos para el uso de los EAAs Protocolo para la Administración de los EAAs entre los Deportistas En la práctica diaria común entre los atletas, éstos combinan una diversidad de esteroides en la forma de preparaciones para consumo oral o vía hipodérmica (Evans & Mcveigh 2008). Los métodos hipodérmicos incluye una preparación basada en aceite o en agua. Para asegurar un efecto ergogénico más potente, los usuarios prefieren emplear los EAAs sintéticos (Graham, Davies, Grace, Kicman, & Baker, 2008). Existe una variedad de dosis para la administración de los esteroides de tipo anabólicos. A este respecto, la dosis puede fluctar de 250 mg hasta 3,200 mg por cada semana (Juhn, 2003). Los atletas usuarios de los EAAs pueden seguir varios tipos de regímenes, que puede ser: 1) método cíclico (cycling), 2) protocolo piramidal (pyramiding), 3) estrategia de aplilamiento (stacking), 4) disminución gradual (tapering), y 5) estabilización (plateauing) (George, 1996; Graham, Davies, Grace, Kicman & Baker, 2008). Por ejemplo, tales deportistas usuarios de esteroides, aumentan de manera progresiva la dosis de esta droga. Esta progresión ocurre en ciclos de seis a doce semanas. Además, tal metodología periodizada para el uso de EAAs se emplea por varios fines, a saber: 1) la prevención de una estado de tolerancia ante tal sustancia, 2) disminuir el latente riesgo de sufrir de los efectos adversos/secundarios por el uso frecuente de esta droga, y 3) permitir que el tiempo tomado por el eje hipotalámico-hipófisis-gónadas restablezca su función biológica normal (Evans & Mcveigh, 2008). Se estima que la dosis neta los esteroides consumidos por los atletas exceden el 40% de la prescrita clínicamente (McArdle, Katch, & Katch, 2010, p. 541). Para evitar que estos deportistas evidencien una prueba de dopaje positiva en esteroides anabolizante, los mismos reducen, de manera progresiva, la dosis consumida previo a los meses donde habrá de llevarse a cabo la competencia deportiva. La tendencia entre los atletas usuarios de EAAs es emplear el método de aplilamiento, puesto que este regimen reduce al mínimo los riesgos clínicos de estas sustancias, mientras optimiza el efecto ergogénico de los protocolos (Graham, Davies, Grace, Kicman & Baker, 2008). Nivel de Efectividad, o Efectos Comprobados, de los EAAs Fundamentado en la evidencia que dispone la literatura científica, ciertamente es cuestionable si realmente los EAAs inducen un efecto de ergogenia. Gran parte de tal controversia establecida en la comunidad científica, con respecto a la validez y confiabilidad de los hallazgos experimentales, se fundamenta en la problemática presente en el diseño y metodología de estas investigaciones. Por ejemplo, varios trabajos de investigación científica analizando la efectividad de los esteroides en la ejecutoria competitiva poseen problemas en los grupos de control, falta de consistencia en el diseño experimental, variaciones en la dosis y duración del tratamiento, problemas en la cuantificación de la intensidad, el uso de suplementos dietéticos empleados en los estudios, la evidencia de una experiencia previa por parte de los sujetos que participan en la investigación, diferencias individuales con respecto a las respuestas de la droga y otros problemas. La presencia de diversas variables contaminantes afectan los resultados en estas investigaciones científicas. Por ejemplo, un factor determinante en los estudios con esteroides anabólicos-androgénicos es el efecto que poseen estas drogas sobre el sistema nervioso autonómico. Se ha evidenciado que los esteroides promueven un estado de Alarma (pelear o huir) entre los atletas. Este tipo de agresividad permite al competidor incrementar su volumen e intensidad del entrenamiento deportivo (McArdle, Katch, & Katch, 2010, p. 542). Tal efecto contaminante puede estar presente en estos estudios. También, deportista puede percibir, erróneamente, que se ha manifestado una adaptación morfofuncional a raíz del entrenamiento deportivo. Una vez mas, tales efectos producen un efecto ergogénico falso, de manera que invalidad los hallazgos del estudio científico. Más aún, ciertas investigaciones científicas estudiando los efectos de los esteroides anabólicos-adrogénicos han demostrado que el uso de estas drogas por los atletas alteran la función psicológica de éstos, como el estado de humor y otros disturbios de tipo psiquiátrico (Clark & Henderson, 2003; Fudala, Weinrieb, Calarco, Kampman & Boardman, 2003; Graham, Davis, Kicman, Covan, Hullin, & Baker, 2007). Otra vertiente, para los hallazgos conflictivos que estudia los efectos ergogénicos de los EAAs, se orienta hacia los estudios con animales y aquellos empleando como sujetos a seres humanos. Por ejemplo, los estudios científicos que emplean como sujetos a una variedad de especies de animales (comúnmente roedores), han mostrado que cuando se acopla el uso de EAAs con el entrenamiento físico, conjuntamente con la ingesta apropiada de sustancias proteínicas, se observa un efecto de tipo anabólico a nivel del tejido muscular(Rogozkin, 1979). Sin embargo, en otro estudio, empleando también roedores como modelo experimental, no se evidenció un efecto de naturaleza anabólico en los músculos esqueléticos de ratas (Max & Rance, 1984). Conflictos similares se han mostrado en investigaciones que emplean seres humanos, mientras un estudio evidenció un incremento en la masa corporal (MC), otros no evidenciaron una respuesta favorable en variales de la aptitud muscular y composición corporal (Forbes, Porta, Herr, & Griggs, 1992). A pesar de tal inconsistencia, existe la tendencia que al incorporar un regimen de EAAs sintéticos en un programa con resistencias, se observa un incremento en la sección transversal de los músculos esqueléticos (i.e., hipertrofia muscular), y mejora la aptitud muscular, específicamente la fortaleza y potencia muscular. Además, bajo estas circunstancias, se experimenta un proceso de recuperación más eficiente, distinguido luego de cada sesión diaria de entrenamiento deportivo (Ej: con resistencias) o competición (Kraemer, Fleck & Deschenes, 2012, p. 422). No obstante, también la literatura científica ha evidenciado los riesgos y efectos secundarios que resultan del uso agudo y crónico de tales hormonas sintéticas (ACSM, 1987; Büttner, & Thieme, 2010; Hoffman, Kraemer, Bhasin, Stover, Ratamess, Haff, Willoughby & Rogol, 2009; Kuipers, H. 1998; NATA, 2012; Warpeha, 2006). El Dilema de la Dosis para los EAAs La confusión continúa en los estudios científicos concerniente a la dosis de los EAAs. En algunos informes de investigación, se sugiere la necesidad de un programa terapéutico de EAAs basado en la prescripción médica, de manera que sea evidente una respuesta morfofuncional a nivel del tejido musculoesqueletal en sujetos que sufren patologías que inducen un efecto de sarcopenia (McArdle, Katch & Katch, 2010, 542-543). Riesgos y Complicaciones Médicas Existe un vasto cuerpo de literatura científica que evidencian una variedad de patalogías, de gran peligro para la salud, a raíz del uso y abuso de los esteroides anabolizantes. Se ha reportado que el uso crónico de EAAs induce a una cadena de efectos secundarios, como lo son: 1) cardiomiopatías; 2) hipertensión (causado por la retensión de sodio y deficiencia en la capacidad vasodilatadora); 4) apolejías (Ej: hemorragias encefálica, problemas isquémicos en el encéfalo); 3) disturbios hepáticos (Ej: hepatoxicidad, neoplasia, colestasis, cálculos biliares, ictericia); 5) problemas hematológicos (Ej: incremento del hematocrito, aumento en los factores de coagulación [i.e, incremento plaquetario, antitrombina III, plasminógeno y del fibrinógeno], con posible riesgo de trombosis); 6) alopecia androgénica en mujeres (disminución gradual en la cantidad, y calidad, de cabello, resultando el calvicie); 7) masculinización, o virilización, en la mujeres (se incluye el hirsutismo facial y corporal, disminución en el tejido de las mamas, enronquecimiento de la voz, alargamiento del clítoris, acné y calvicie masculina); 8) feminización en los varones (manifestado por la reducción en la secreción de testosterona, ginecomastía, i.e., agrandamiento de las glándulas mamarias, y atrofia testicular); 9) disfunción reproductiva (Ej: disminución en la ovulación, reducción en la secreción de estrógeno, oligospermia [secresión seminal deficiente] o azoospermia [ocasionando infertilidad en la población masculina]); 10) elevación de la lipoproteína de baja densidad o colesterol malo (low density lipoprotein, LDL o LDL-C); 11) disminución de la lipoproteína de alta densidad o colesterol bueno (high density lipoprotein, HDL o HDL-C), mediado por la enzima lipoproteinlipasa hepática; 12) deterioro del tejido conectivo de los músculos esqueléticos; 13) ruptura de los tendones (debido al exceso en la hipertrofia muscular); 14) trastornos endocrinos (Ej: hipotiroidismo, mayor resistencia a la insulina, incremento en la producción y liberación de la hormona de crecimiento [growth hormone o GH], irregularidades menstruales que surgen por disturbios en la secreción de gonadotropinas); 15) disturbios metabólicos (Ej: incremento en la masa corporal [MC] ); 16) inflamación prostática; 17) afecciones dermatológicas (Ej: acné, estrías dermatológicas); 18) hipertrofia fálica (agrandamiento del pene) en niños; 19) estancamiento del crecimiento lineal en la población pediátrica (debido a la cierre prematura de las placas epifisarias a nivel de los huesos largos [posiblemente por la aromatización a estrógenos]); 21) Ictericia; 22) alteraciones psicológicas y psiquiátricas (Ej: agresión y violencia, ansiedad, depresión, dependencia); 23) dependencia física (a esta sustancia), entre otras (Berg, Tymoczko, Stryer & Gatto, 2012, p. 948; Brunton, Parker, Blumenthal, & Buxton, 2008, p. 1020; Büttner & Thieme, 2010; Cantabrana, Hidalgo & Sánchez, 2009; Casavant, Blake, Griffith, Yates, & Copley, 2007; Colado & Alguacil, 2009; Hartgens & Kuipers, 2004; Kanayama, Brower, Wood, Hudson & Pope, 2009; Sari, 2010; Evans & Mcveigh, 2008; McArdle, Katch, & Katch, 2010, p. 543; Vanberg & Atar, 2010; Weiss, 2012, p. 158; Wood, 2008). El uso, y abuso, crónico, y de alta dosis, de los EAAs puede resultar en un deterioro relativamente permanente con respecto de las funciones biológicas normales de la testosterona (McArdle, Katch, & Katch, 2010, p. 543). Estudios científicos con roedores han evidenciado a largo plazo tumores hepáticos y renales, linfosarcomas y patología cardiaca. Tales enfermedades mortales han reducido significativamente la expectativa de vida de los ratones (McArdle, Katch, & Katch, 2010, p. 543). Como se mencionó en el párfo anterior, la población femenina ha experimentado problemas de salud de cuidado, como lo son la virilización, alteración del crecimiento normal de los huesos largos, disturbios menstruales, hirsutismo (crecimiento anormal de vello corporal y facial), marcado aumento en las glándulas sebáceas, hipertrofia del clítoris, disminución en el tamaño de los senos, alopecia, acné, un tono de voz más grave y otros. Ciertos disturbios hormonales son evidente con el uso de EAAs, estos incluyen reducción en los niveles sanguíneos de la hormona luteinizante (LH, siglas en inglés) la hormona estimulante del folículo (FSH, siglas en inglés) y las hormonas regulares secretadas por los ovarios (Ej: progesterona y estrógeno). Consecuentemente, tales alteraciones endocrinas, vinculadas con la función reproductora femenina, afectan adversamente los procesos normales que ocurren en los ovarios, como lo son la maduración folicular, la ovulación y la actividad de la menstruación. Aunque no se ha comprobado conclusivamente, si la atleta femenina persiste en el consumo de EAAs, entonces tal comportamiento puede resultar en esterilidad (Büttner & Thieme, 2010). El gobierno federal de los Estados Unidos Continentales ha expuesto un documento, de libre acceso, que indica los peligros para la salud que resulta por el uso frecuente de EAAs (National Institute of Drug Abuse [NIDA], 2012). Esta literatura expone que el consumo de andrógenos sintéticos conllevan a disturbios hepáticos (hígado), icteria (color amarillento de ciertos tejidos o líquidos del organismo humano y la piel), retención de líquidos, hipertensión (alta presión arterial), incremento en la LDL-C, disminución en la lipoproteína de alta densidad o colesterol bueno (high density lipoprotein, HDL o HDL-C), fallo renal, acné severo y extremidades temblorosas (Ej: las manos). Además, se han evidenciado efectos adversos específicos, por el uso de EAAs, en la población femenina, varonil y en adolescentes. Para los hombres, el abusos de los EAAs resultó en atrofia de los testículos, disminución en el conteo de esperma, impotencia (infertilidad), alopecia (caída de cabello), telarquia (desarrollo de senos) y un mayor riesgo para la adquisión de un neopalsma maligno (cáncer) a nivel de la próstata. Para el colectivo femenido, los efectos secundarios consisten en hirsutismo (crecimiento de vello facial), alopecia, disturbios menstruales (Ej: amenorrea o pérdida del periodo menstrual), hipertrofia del clitoris y desarrollo de un voz más grave. Por el otro lado, el uso continuo de los EAAs entre los adolescentes puede ocasionar un retardo en el crecimiento longitudinal de sus dimensiones corporales. Esta afección se debe a una maduración prematura, lo cual, a su vez, produce una pubertad acelerada. Existe un riesgo para adquirir el síndrome de inmunodeficiencia adquirida (SIDA) en aquellos casos donde de inyectan los EAAs. Más aún, tal práctica puede resultar en un grave daño al hígado, oacasionado por hepatitis. Mercado Peligroso de los EAAs Educar a los atletas sobre los riesgos clínicos por el uso crónico de los EAAs es la mejor opción que existe en la actualidad (Leone & Becker, 2008). El problema es que a través de la Internet/Web existe un medio fácil de aceder a estas peligrosas sustancias. Esto se complica porque muchas de tales compañias no detallan a cabalidad las complicaciones médicas que se derivan por el uso de estas sustancias. Más aún, la dosis sugerida por estas agencias virtuales representan el doble de lo recomendado en circusntancias terapéuticas (Cordaro, Lombardo & Cosentino, 2011). Conclusión Aunque existe una variedad de investigaciones científicas que dispoden de hallazgos contradictorios, la tendencia de los efectos ergogénicos por parte de los EAAs exógenos, se pueden limitar a un incremento en la MCA y en la fortaleza muscular. No obstante, la literatura científica nos indica que existen riegos que pueden atentar contra la salud de los usuario de tales sustancias. Además, según lo discutido previamente, los EAAs se encuentran prohibidos en la mayoría de las competencias deportivas a nivel internacional y olímpicas. Entonces, los esteroides anabolizantes, en definitiva, son ilegales y no éticos, de manera que su uso no es recomendado. ESTEROIDES SUSTITUTOS Otro grupo de equivalentes hormonales de tipo esteroides poseen un gran arraigo entre los atletas usuarios frecuentes de agentes anabólicos. Una de las razones para tal auge es que, para aquellos atletas que consumen de forma regular los EAAs durante su entrenamiento físico, el sustituto esteroide sirve de transición al aproximarse el periodo competitivo del atleta. Otra ventaja de estos elementos entre los deportistas, es la fácil disponibilidad de los mismos. Por ejemplo, tales fármacos se encuentran en diversos establecimientos comerciales que venden productos orgánicos y en otros enfocados hacia la distribución de una gran variedad de vitaminas y minerales. Además, es posible ordenar por correo tales productos mediante la Internet/Web, o revistas populares especializadas en el tópico de desarrollo muscular. También, una forma de acceso común para estos esteroides sustitutos consiste en un canal de distribución ilegal, regularmente conocido como el “mercado negro”. Clenbuterol Uso por los Atletas Esta sustancia representa un amino simpaticomimético (estimulante), conocido con los nombres comerciales de Prontovent, Spiropent, Clenasma, Novegan y Monores. Su propuesto beneficio se fundamenta en un efecto anabólico de los tejidos proteínicos (Ej: músculos esqueléticos) y disminución en el tejido graso (McArdle, Katch, & Katch, 2010, p. 545). Tal compuesto se utiliza con frecuencia para prevenir pruebas de dopaje positivas al uso de EAAs a través del transcurso de la etapa competitiva. Para este colectivo de atletas, clenbuterol solo permite una pérdida mínima con respecto a la masa musculoesqueletal. Además, el organismo humano opta por los ácidos grasos como sustrato metabólico, lo cual incrementa la MCA (Prather, Brown, North & Wilson, 1995). Consecuentemente, para aquellos atletas fisiculturistas, se observa una mayor definición corporal a nivel de los músculos esqueléticos. Más aún, estos agentes son populares entre la población femenina, pues no son muy evidentes las respuestas androgénicas, en comparación con las EAAs (McArdle, Katch, & Katch, 2010, p. 545). Farmacología Clenbuterol forma parte de un conjunto de constituyentes farmacológicos, como lo son albuterol, clenbuterol, formoterol, terbutalino, salbutamol y salmeterol. El mismo se categoriza como un agonista ß2-adrenérgico (Brunton, Parker, Blumenthal, & Buxton, 2008, pp. 159-161). Entonces, tal sustancia favorece la afinidad de los receptores adrenérgicos con respecto a las catecolaminas séricas (Ej: epinefrina y norepinefrina), así como a otros compuestos del grupo amino adrenérgico. Indicaciones Terapéuticas El clenbuterol es indicado como broncodilatador, particularmente en pacientes con asma bronquial (Brunton, Parker, Blumenthal & Buxton, 2008, p. 160; Flinn, 2005). Tal estimulante ha sido empleado para incrementar el nivel de proteínas, así como la disminución en la masa corporal grasa (MCG), de ciertos animales, como lo son las vacas, el ganado y las obejas (Kuhn, Swartzwelder & Wilson, 2003, pp. 101-102). Además, como estrategia terapéutica, clenbuterol se ha prescrito en animales con el fin de minimizar las consecuencias musculares de la sarcopenia originada por edad avanzada (i.e., envejecimiento) (Dupont-Versteegden, 1996; Zeman, Zhang & Etlinger, 1994). También, tal químico se ha empleado, de manera experimental, a reducir la pérdida de tejido magro (músculo esquelético) que resulta de patologías particulares (Ej: HIV), periodos prolongados de inmovilización, estados de inanición, disturbios anoréxicos y bulímicos, entre otras circunstancias. Posibles Manifestaciones Ergogénicas Tocante a los usos clínicos de clenbuterol, en animales y seres humanos, se ha evidenciado que tales ß2-adenérgicos manifiestan acciones anabólicas (aumento en la masa muscular) a nivel de los músculos esqueléticos de los animales (Dupont-Versteegden, 1996; Zeman, Zhang & Etlinger, 1994). Los hallazgos de estudios científicos con el ganado han mostrado que, posterior a la administración de altas dosis de clenbuterol, se observó que tales animales experimentaban un incremento en el depósito de proteína a nivel de los músculos esqueletales y cardiaco, y un mayor estímulo al catabolismo de las reservas de lípidos. Cuando se duplicó el protocolo experimental a la población equina, fue evidente un incremento de la MCA (Kearns, McKeever, Malinowski, Struck & Abe, 2001). Otras investigaciones han encontrado un incremento en ciertos tipos de fibras musculares, específicamente de Tipo II (Criswell, Powers & Herb, 1996). Posiblemente tal respuesta musculoesqueletal de tipo anabólica (i.e., hipertrofia muscular), responde al catabolismo proteínico y a un mayor estímulo para el anabolismo de las proteínas (Agbenyega & Wareham, 1990; Benson, Foley-Nelson, Chance, Zhang, James, & Fischer, 1991). En mujeres, estos tipos de agentes farmacológicos no han comprobado un efecto de naturaleza anabólica, aunque se ha observado un mejor rendimiento en la actividad anaeróbica (Panse, Arlettaz, Portier, Lecoq, Ceaurriz, & Collomp, 2006). En otros informes de la literatura científica que han utilizando como modelo roedores, se ha evidenciado que, al consumir clenbuterol en combinación con un programa de entrenamiento físico, el efecto de tipo anabólico sobre la masa de los músculos esqueléticos es de mayor magnitud cuando no se posee una experiencia previa en entrenamiento, al compararse con el grupo que cuenta con un entrenamiento físico desde el principio (Murphy, Béliveau, Seburn & Gardiner, 1996). Efectos Secundarios Manifestacione clínicas al uso de agonistas beta 2 adrenérgicos. Los signos comunes incuyen temblores, anorexia, taquicardia, arritmias cardiacas peligrosas e hipertrofia del músculo cardiaco (Flinn, 2005; Kuhn, Swartzwelder & Wilson, 2003, p. 102; Prather, Brown, North & Wilson, 1995). Por el otro lado, los síntomas observados son palpitaciones, ansiedad, cefalgia (dolor de cabeza) e insomnio (Flinn, 2005). Otros problemas patolológicos incluyen una mayor fragilidad ósea (Bonnet, Benhamou, Beaupied, Laroche, Vico, Dolleans & Courteix, 2007; Bonnet, Brunet-Imbault, Arlettaz, Horcajada, Collomp, Benhamou & Courteix, 2005) y el agrandamiento de la aorta (Sleeper, Kearns, & Mckeever, 2002). Más aún, en un estudio con animales (población equina) se evidenció que clenbuterol posee un efecto de tipo ergolítico sobre la ejecutoria competitiva de naturaleza aeróbica (Kearns & Mckeever, 2002). Con el uso desmedido de estos agentes, se han reportado complicaciones clínicas que pueden ser mortales, como lo son un infarto al miocardio (ataque cardiaco) o apolejía (Prather, Brown, North & Wilson, 1995). Carne contaminada con clenbuterol. Una práctica común es prescribir esta sustancia en el ganado vacuno joven, el cual se acumula principalmente en el hígado. Como resultado, se han reportado intoxicaciones de clenbuterol en humanos, luego del consumo de vísceras de estos animales (Marban-Arcos & López-Jiménez, 2011). Otros Tipos de Agonistas Beta 2 Adrenérgicos Uso por los Atletas En ambiente deportivo, se ha detectado que un grupo de competidores emplean otros tipos de agonistas ß2-adrenérgicos, de naturaleza simpatomiméticos, como lo son metaproterenol, albuterol, salbutamol, y otros similares (McArdle, Katch, & Katch, 2010, p. 546). Posibles Manifestaciones Ergogénicas Con lo que respecta al fármaco albuterol, los estudios indican una acción de ergogenia cuando el grupo experimental no se encuentra bajo entrenamiento físico. Entonces, a este respecto, se ha observado que tal químico promueve la potencia muscular, según fue establecido en una prueba máxima en el cicloergómetro de 15 segundos (s) en duración (Signorile, Kaplan, Applegate & Perry, 1992). Posiblemente, el estímulo que dispone el albuterol sobre los receptores ß2-adrenérgicos a nivel de los musculos esqueléticos no entrenados provea la explicación para la mayor capacidad de éstos para generar una fuerza y potencia maxima (McArdle, Katch, & Katch, 2010, p. 546). En términos generales, los agonistas ß2 inhalados no han evidenciado una respuesta de ergogenia significativa en aquellos competidores que no son asmáticos (Kindermann, 2007; Wolfarth, Wuestenfeld & Kindermann, 2010). Conclusión Posiblemente, algunos agonistas ß2-adrenérgicos (Ej: clenbuterol) promuevan la síntesis e hipetrofia muscular, y una disminición en la MCG. No se ha evidenciado que esta sustancia incremente fortaleza muscular. Esto implica que solo poseen efectos de imagen corporal, de los cuales solo se benfician los fisiculturistas. Por el otro lado, otros tipos de.ß2-adrenérgicos solo disponen de algun incentivo para ciertas ejecutorias anaeróbicas-explosivas en sujetos no entrenados. En lo que respecta a los agonistas ß2 inhalados, no se han reportado respuestas de tipo ergogénicas. Finalmente, existen varios efectos clínicos significativos que resultan del consumo de agentes agonistas ß2-adrenérgicos, particularmente el clenbuterol. HORMONA DE CRECIMIENTO A la hormona de crecimiento (Growth Hormone, GH, siglas en ingles) se le conoce también con el nombre de hormona de crecimiento humana (Human Growth Hormone, HGH o hGH, siglas en ingles), somatotrofina u hormona somatotrófica (Somatotropic Hormone, STH, siglas en ingles) (Goodman, 2003, p. 56). Al estado sintético de esta hormona, se le otorga el nombre de hormona del crecimiento humana recombinante (Recombinant Human Growth Hormone o rhGH), pues emplea la tecnología de ADN recombinante (Bryant, Baxter, Cave & Milne, 2007; Williams, 1998, p. 214). Tal forma sintética solo se puede administrar vía hipodérmica (Juhn, 2003). Para los años previo al 1985, el acceso a la hGH exógena solo era posible a través de extractos de la pituitaria halladas en cadáveres (Wadler & Hainline, 1989, p. 70). Acciones Farmacológicas de la rhGH La somatotrofina la secreta el lóbulo anterior de la hipófisis (o pituitaria), es decir, la adenohipófisis. Para la mayoría de los tejidos en el organismo humano, la hGH posee las siguientes acciones: 1) estimula la síntesis de proteína; 2) promueve la utilización de los ácidos grasos libres (AGL o Free Fatty Acids, FFA, siglas en ingles); 3) promueve la manufactora del factor de crecimiento insulínico tipo 1 o "Insulin-like Growth Factor 1" (IGF-1 o somatomedina C); 4) inhibe la utilización de glucosa; y 5) promueve el crecimiento en general de la masa corporal (MC) y la talla (crecimiento lineal) en niños y adolescentes (Bidlingmaier & Strasburger, 2010; Goodman, 2003, p. 57). La hormona de crecimiento se encuentra regulada por varias hormonas liberadas desde el hipotálamo, conocidos como factores hipotalámicos, que inhiben o estimulan la liberación de la hGH por la hipófisis (Underwood & Van Wyk, 1989)). Por ejemplo, la hormona liberadora de la hormona de crecimiento (Growth Hormone-Releasing Hormone o GHRH, siglas en ingles) promueve la generación y liberación de la hGH a nivel de la adenohipófisis. Su contraparte, el factor inhibidor para la liberación de la somatotrofina (Somatotropin Releasing-Inhibiting Factor o SRIF, siglas en ingles), o la hormona inhibidora de la hormona de crecimiento (Growth Hormone Releasing-Inhibiting Hormone o GHIH, siglas en ingles), ejerce el efecto inverso de la GHRH. Además, la hormona conocida con el nombre de grelina (ghrelin) promueve la síntesis, y liberación, de la hGH al estimular las células somatotropas, ubicadas en el lóbulo anterior de la hipófisis. Tal acción produce un efecto aumentado de las GHRH. También, la grelina estimula la producción de la hormona de crecimiento mediante la acción directa sobre las células neurosecretoras del hipotálamo para que generen la GHRH (Goodman, 2003, p. 66). DOPAJE SANGUÍNEO Las manipulaciones hematológicas de los atletas que dependen de una alta capacidad de tolerancia cardiorrespiratoria se han reportado desde muchos años atrás en los países nórdicos. Comúnmente, el dopaje sanguíneo consiste en transfundirse la propia sangre del competidor o la de un donador compatible. En la actualidad, existen diversas variantes para el dopaje sanguíneo (Joyner, 2002; Lippi, Franchini, Salvagno, & Guidi, 2006). En ocasiones, estos protocolos se pueden combinar con un entrenamiento físico en ambientes hipobáricos (i.e., circunstancias hipóxicas, como por ejemplo la altitud), la administración de eritropoyetina (EPO) o sus productos análogos (Reichel, & Gmeiner, 2010), la infusión de substitutos sanguíneos (Ej: transportadores de oxígeno basados en la hemoglobina) (Giraud, Sottas, Robinson & Saugy, 2010), suplementación nutricional (Ej: hierro), y dopaje genético (Ej: transfección genética de la eritropoyetina humana) (Azzazy, 2010; Baoutina, 2011). El efecto ergogénico reclamado por este tipo de dopaje es mejorar la capacidad para el transporte de oxígeno, principalmente por medio de un aumento en la concentración de la hemoglobina (Hb) sérica. Se espera que este efecto ayude al rendimiento de eventos que requieren una alta capacidad aeróbica. Clasificación La presente manipulación hematológica en deportistas de tolerancia se conoce también con el nombre de eritrocitemia inducida. Como fue mencionado previamente, existen dos maneras de proceder con este tipo de dopaje (Williams, 1998, p. 141). El primero consiste en la transfusión homólogo de sangre por parte de un individuo que sea compatible con el atleta que requiere el dopaje. En la otra alternativa, el competidor recipiente se transfunde su propia sangre, conocido con el nombre de transfusión autólogo. Tal material hematológico fue previamente extraído del atleta, y congelado, durante su entrenamiento pico. El volumen de sangre transfundido varía de 500 mililitros (mL) a 2 litros (L) (Williams, 1998, p. 141). Meta del Dopaje Sanguíneo Se espera que la transfusión de sangre en estos atletas incrementen la potencia aeróbica en competencias que demandan una elevada tolerancia cardiorrespiratoria, como los son las carreras pedestres de larga distancia (CPLD), eventos de ciclismo de prolongadas distancias, competencias de tríalos, eventos de esquí de campo traviesa, entre otros. Protocolo del Dopaje Sanguíneo Tradicionalmente, este tipo de dopaje ha consistido de extraer la propia sangre del competidor (alrededor de 450 a 1800 mL) durante el pico de su etapa precompetitiva. Luego de someterse la sangre a un proceso de centrifugación, la misma se almacena a bajas temperaturas (de 4°C a hasta un estado de congelación) (Lippi, Franchini, Salvagno, & Guidi, 2006; McArdle, Katch, & Katch, 2010, p. 566). Posteriormente, faltando de uno a siete día para el evento competitivo de tolerancia, el atleta se transfunde esta sangre (McArdle, Katch, & Katch, 2010, p. 566). Mecanismo Fisiológico concerniente al Efecto Ergogénico que Propone el Protocolo del Dopaje Sanguíneo En teoría, la transfusión de sangre aumenta la concentración del recuento de los eritrocitos en la sangre y, por ende, también la hemoglobina, hasta un 20 % (Lippi, Franchini, Salvagno, & Guidi, 2006). Fundamentado en este efecto, se espera que los deportistas que participan en eventos de tolerancia (sobre cinco minutos) mejoren su capacidad para transportar el oxígeno hacia los músculos activos, de manera que se experimente un incremento en la producción oxidativa (aeróbica) de energía (en la forma de adenosina triosfatada, o ATP). Entonces, el resultado neto sería una mejor ejecutoria competitiva en tales eventos. Nivel de Efectividad del Dopaje Sanguíneo La evidencia de la literatura científica nos indica que, en efecto, el dopaje sanguíneo permite que el atleta mejore su rendimiento en competencias de naturaleza aeróbica (Williams, 1998, p. 142). Se establece que la concentración de Hb aumente posterior a la infusión de un volumen de sangre, o glóbulos rojos, de aproximadamente 900-2,000 mL. Consecuentemente, los hallazgos de estos estudios científicos han demostrado que paralelamente incrementa la masa de los glóbulos rojos y en el contenido total sérico del oxígeno (Williams, 1998, p. 142). A raíz de estos efectos, se facilita el sistema de transporte de oxígeno, lo cual aumenta la capacidad oxidativa del atleta para generar energía. Como resultado, también se incrementa el consumo de oxígeno máximo (VO2máx). Riesgos y Complicaciones Médicas Esta práctica puede resultar en una variedad de disturbios medicos. En el caso del dopaje sanguíneo que emplea la transfusión homóloga, el competidor puede contraer algunos tipos de infecciones hepáticas, e inclusive el síndrome de inmunodeficiencia adquirida ( SIDA o HIV, siglas en inglés) (Williams, 1998, p. 142). Aunque el riesgo se reduce al atleta transfundirse su su propia sangre, la ausencia de un control de calidad durante este procedimiento puede conllevar a graves patologías. Por ejemplo, existe el riesgo que al transfundirse la propia sangre del deportista aumente el nivel de su viscosidad sanguínea, lo cual puede producir alteraciones hemodinámicas adversas (Lippi, Franchini, Salvagno, & Guidi, 2006). Además, las investigaciones científicas han evidenciado otros disturbios clínicos, como lo son embolias pulmonares, infección bacterial, septicemia, flebitis y otras (Ghaphery, 1995). Perspectiva Ética y Legal No se considera aceptable que los deportistas realicen este tipo de dopaje, pues éstos no estarían compitiendo a un nivel equitativo y justo. La comunidad Olímpica ha prohibido el uso del dopaje sanguíneo desde el 1985 (Williams, 1998, p. 143). Conclusión Los estudios han revelado que las transfusiones de sangre disponen de un mejor sistema de transporte de oxígeno y, como resultado, aumenta la efectividad de la ejecutoria competitiva durante aquellos eventos que dependen de una elevada tolerancia aeróbica. No obstante, debido a que tal práctica no es ética y el COI prohibe cualquier variedad de dopaje sanguíneo, es necesario que los atletas no incurran en esta manipulación hematológica. REFERENCIAS Agbenyega, E. T., & Wareham, A. C. (1990). Effect of clenbuterol on normal and denervated muscle growth and contractility. Muscle Nerve, 13(3), 199-203. American College of Sports Medicine
[ACSM] (1987). Position stand on the use of anabolic-androgenic steroids in
sports. Medicine & Science in Sports & Exercise, 19(5), 534-539.
Recuperado de
http://journals.lww.com/acsm-msse/Citation/1987/10000/Position_Stand_on_The_Use_of_Anabolic_Androgenic.23.aspx American College of Sports Medicine
[ACSM], American Dietetic Association [ADA], & Dietitians of Canada [DC] (2009).
Nutrition and Athletic Performance: a Joint Position Statement. Medicine &
Science in Sports & Exercise, 41(3), 709-731. Recuperado de
http://journals.lww.com/acsm-msse/Fulltext/2009/03000/Nutrition_and_Athletic_Performance.27.aspx Agencia Mundial Antidopaje [AMA] (2012). El Código Mundial Antidopaje. La Lista de Prohibiciones 2012: Estándar International. Recuperado de http://www.wada-ama.org/Documents/World_Anti-Doping_Program/WADP-Prohibited-list/2012/WADA_Prohibited_List_2012_ES.pdf Agencia Mundial Antidopaje [AMA] (2009). Código Mundial Antidopaje. Recuperado de http://www.wada-ama.org/static/PDF/OtherLanguages/code_v2009_Sp.pdf Azzazy, H. M. E. (2010). Gene doping. En E. Thieme, & P. Hemmersbach (Eds.), Handbook of Experimental Pharmacology 195: Doping in Sports (pp.485-512). New York: Springer-Verlag Berlin Heidelberg. Recuperado http://www.anabolicsteroidcalculator.com/resources/articles/ebooks/doping/chapter20.pdf Baoutina, A. (2011). Chapter 32: Performance enhancement by gene doping. En C. Bouchard & E. P. Hoffmany (Eds.), Genetic and Molecular Aspects of Sports Performance (pp. 373-383). Hoboken, NJ: Wiley-Blackwell. Benson, D. W., Foley-Nelson, T., Chance, W.T., Zhang, F.S., James, J.H., & Fischer, J. E. (1991). Decreased myofibrillar protein breakdown following treatment with clenbuterol. The Journal of Surgical Research, 50(1), 1-5. Berg, J. M., Tymoczko, J. L., Stryer, L., & Gatto, G. J. (2012). Biochemistry (7ma. ed., pp. 780, 948). New York: W. H. Freeman and Company. Bidlingmaier, M., & Strasburger, C. J. (2010). Growth hormone. En E. Thieme, & P. Hemmersbach (Eds), Handbook of Experimental Pharmacology 195: Doping in Sports (pp. 187-200). New York: Springer-Verlag Berlin Heidelberg. Recuperado de http://www.anabolicsteroidcalculator.com/resources/articles/ebooks/doping/chapter8.pdf Bonnet N, Benhamou, C. L., Beaupied, H., Laroche, N., Vico, L., Dolleans, E., & Courteix, D. (2007). Doping dose of salbutamol and exercise: deleterious effect on cancellous and cortical bones in adult rats. Journal of Applied Physiology, 102(4):1502-1509. Recuperado de http://jap.physiology.org/content/102/4/1502.long Bonnet, N., Brunet-Imbault, B., Arlettaz, A., Horcajada, M. N., Collomp, K., Benhamou, C., L., & Courteix, D. (2005). Alteration of trabecular bone under chronic [beta]2 agonists treatment. Medicine & Science in Sports & Exercise, 37(8), 1493-1501. Recuperado de http://journals.lww.com/acsm-msse/Fulltext/2005/09000/Alteration_of_Trabecular_Bone_under_Chronic.7.aspx Bryant, J., Baxter, L., Cave, C. B., & Milne, R. (2007). Hormona de crecimiento recombinante para la baja talla idiopática en niños y adolescentes. La Bibblioteca Cochrane Plus. Recuperado de http://www.update-software.com/bcp/bcpgetdocument.asp?documentid=cd004440 Brunton, L. L., Parker, K. L., Blumenthal, D. K., & Buxton, I. L. O. (2008). Goodman & Gilman's Manual of Pharmacology and Therapeutics (pp. 159-161, 1012, 1017, 1019-1021). New York: MacGraw-Hill Companies, Inc. Büttner, A., & Thieme, D (2010). Side Effects of anabolic androgenic steroids: Pathological findings and structure–activity relationships. En E. Thieme, & P. Hemmersbach (Eds.), Handbook of Experimental Pharmacology 195: Doping in Sports (pp. 459-484). New York: Springer-Verlag Berlin Heidelberg. Recuperado de http://www.anabolicsteroidcalculator.com/resources/articles/ebooks/doping/chapter19.pdf Cantabrana, B., Hidalgo, A., & Sánchez, M. (2009). Esteroides sexuales, anabolizantes y anticonceptivos. Farmacología uterina. En P. Lorenzo, A. Moreno, I. Lizasoain, J. C., Leza, M. A., Moro, & A. Portolés (Eds), Velázquez Farmacología Básica y Clínica (pp. 645-673). Argentina, Buenos Aires: Editorial Médica Panamericana. Casavant, M. J., Blake, K., Griffith, J., Yates, A., & Copley L. M. (2007). Consequences of use of anabolic androgenic steroids. Pediatrics of Clinics of North America, 54(4),677-590. Recuperado de http://xa.yimg.com/kq/groups/19520777/1938285377/name/Consequences%20of%20Use%20of%20Anabolic%20Androgenic%20Steroids.pdf Clark A. S., & Henderson, L. P. (2003). Behavioral and physiological responses to anabolic-androgenic steroids. Neuroscience and Biobehavior Review, 27(5), 413-436. Recuperado de http://www.dartmouth.edu/~psych/docs/nbrreview.pdf Colado, M. I., & Alguacil, L. F. (2009). Drogas de abuso. En P. Lorenzo, A. Moreno, I. Lizasoain, J. C., Leza, M. A., Moro, & A. Portolés (Eds.), Velázquez Farmacología Básica y Clínica (pp. 335-353). Argentina, Buenos Aires: Editorial Médica Panamericana. Cordaro, F. G., Lombardo, S. S., & Cosentino, M. M. (2011). Selling androgenic anabolic steroids by the pound: identification and analysis of popular websites on the Internet. Scandinavian Journal Of Medicine & Science In Sports, 21(6), e247-e259. Recuperado de la base de datos de EBSCOhost (SPORTDiscus with Full Text). Criswell, D. S., Powers, S. K, & Herb, R. A. (1996). Clenbuterol-induced fiber type transition in the soleus of adult rats. European Journal of Applied Physiology and Occupational Physiology, 74(5), 391-396. Dupont-Versteegden, E. E. (1996). Exercise and clenbuterol as strategies to decrease the progression of muscular dystrophy in mdx mice. Journal of Applied Physiology, 80(3), 734-741. Eichner E. R.(1993). Ergolytic drugs in medicine and sports. American Journal of Medicine, 95(2), 205-2011. Abstract recuperado de la base de datos de PubMed - indexed for MEDLINE (No. de acceso PMID: 8430716), de http://www.ncbi.nlm.nih.gov/pubmed/8430716 Eichner, E. R. (1986). Ergolytic drugs. Sports Science Exchange, 2(15), 1-4 Eugenio, L. P. (2012). El deporte y la ergogenia: una mirada desde la bioética. Revista Médica Clínica Las Condes, 23(3), 349-354. Recuperado de la base de datos de EBSCOhost (MedicLatina). Evans, M. J., & Mcveigh, J. (2008). An introduction to anabolic steroids. Sportex Medicine, (38), 20-26. Recuperado de la base de datos de EBSCOhost (SPORTDiscus with Full Text). Fahey, T. D. (2005). Weight Training Basics: A Complete Guide for Men and Women (p. 173-174). New York: McGraw-Hill. Recuperado de la base de datos de EBSCOhost (eBbook Collection). Federación Española de Medicina del Deporte [FEMEDE] (s.f.). Declaración del uso de drogas. Recuperado de http://www.femede.es/popup.php?/OtrosDocumentos/DeclaracionDrogas Federación Internacional de Medicina
del Deporte [FIMS] (s.f). FIMS Position Statement. Statement on doping in sport.
Recuperado de
http://www.fims.org/content/assets/documents/PositionStatements/PS13-Statement-on-Doping-in-Sport.pdf Fields, J. , & Turner, J. L. (2009). Performance-enhancing sports supplements. En R. M. Buschbacher, N. D. Prahlow, & S. J. Dave (Eds.), Sports Medicine and Rehabilitation: A Sports-Specific Approach (2da. ed., pp. 39-49). Philadelphia: Lippincott Williams & Wilkins. Flinn, S. B. (2005). Medications and ergogenics. En F. G. O'Connor, R. E. Sallis, R. P. Wilder, & P. S. Pierre (Eds.), Sports Medicine: Just the Facts (pp. 416-426). New York: McGraw-Hill, Medical Pub. Division. Recuperado de la base de datos de EBSCOhost (eBbook Collection) Forbes, G. B, Porta, C. R., Herr, B. E., & Griggs, R. C. (1992). Sequence of changes in body composition induced by testosterone and reversal of changes after drug is stopped. Journal of American Medical Association, 267(3), 397-399. Fudala, P., Weinrieb, R. M., Calarco, J. S., Kampman, K. M., & Boardman, C. (2003). An evaluation of anabolic-androgenic steroid abusers over a period of 1 year: seven case studies. Annals of Clinical Psychiatry, 15(2),121-125 García-Arjona, N., & Bodin, D. (2011). Editorial: Dopaje y ciencias del deporte: ¿Línea de investigación emergente o consolidada? Revista Internacional de Ciencias del Deporte, 7(26), 339-340. doi:10.5232/ricyde2011.026 Garrett, R. H., & Grisham, C. M. (2013). Biochemistry (5ta. ed., pp. 248-249). Boston, MA: Brooks/Cole Cengage Learning. George, A. (1996). The anabolic steroids and peptide hormones. En D. R. Mottran (Ed.), Drugs in Sport (pp. 173-218). New York: E & FN Spon. Ghaphery N. A. (1995). Performance-enhancing drugs. Orthopedic Clinical North America, 26(3),433–442. Giraud, S., Sottas, P-E., Robinson, N., & Saugy, M. (2010). Blood transfusion in sports. En E. Thieme, & P. Hemmersbach (Eds), Handbook of Experimental Pharmacology 195: Doping in Sports (pp. 295-304). New York: Springer-Verlag Berlin Heidelberg. Recuperado de http://www.anabolicsteroidcalculator.com/resources/articles/ebooks/doping/chapter13.pdf Goodman, H. M. (2003). Basic Medical Endocrinology (3ra. ed., pp. 56-57). New York: Academic Press. Recuperado de la base de datos de EBSCOhost (eBbook Collection). Griffin, J. E., & Wilson, J. D. (1989). Trastornos de los testículos y del aparato masculino. En J. D. Wilson, &D. W. Fosted (Eds.), Williams Endocrinología (7ma. ed., pp. 389-463). Argentina, Buenos Aires: Etidorial Médica Panamericana S. A. Graham, M. R., Davies, B., Grace, F. M., Kicman, A., & Baker, J. S. (2008). Anabolic steroid use. Sports Medicine, 38(6), 505-525. Recuperado de la base de datos de EBSCOhost (SPORTDiscus with Full Text). Graham, M. R., Davis, B., Kicman, A., Covan, D., Hullin, D., & Baker, J. S. (2007). Recombinant human growth hormone in abstinent androgenic-anabolic steroid use: Psychological, endocrine, and trophic factor effects. Current Neurovascular Research, 4, 9-8. Hartgens, F. F., & Kuipers, H. H. (2004). Effects of androgenic-anabolic steroids in athletes. Sports Medicine, 34(8), 513-554. Recuperado de la base de datos de EBSCOhost (SPORTDiscus with Full Text). Haupt, H. A., & Rovere, G. D. (1984). Anabolic steroids: A review of the literature. American Journal of Sports Medicine, 12, 469-484. Hoffman, J. R., Kraemer, W. J., Bhasin, S., Storer, T., Ratamess, N. A., Haff, G. G., Willoughby, D. S., & Rogol, A. D. (2009). Position stand on Androgen and human growth hormone use. Journal of Strength and Conditioning Research, 23(5 Suppl), S1–S59. Recuperado de http://www.nsca-lift.org/WorkArea/DownloadAsset.aspx?id=1156 International Association of Athletics Federations [IAAF] (s.f.). Part 1: Drugs in sports. Recuperado de http://www.iaaf.net/mm/Document/imported/42026.pdf International Olympic Committee. (2012). Anti-Doping Rules applicable to the Games of the XXX Olympiad, London 20012. Recuperado de http://www.olympic.org/Documents/Games_London_2012/Anti-doping/IOC_Anti-Doping_Rules_London%20_2012-eng.pdf Joyner, M. J. (2002). Altitude
training, erythropoietin, and blood doping. Exercise & Sport Sciences
Reviews, 30(3), 97-98. Recuperado de
http://journals.lww.com/acsm-essr/Fulltext/2002/07000/Altitude_Training,_Erythropoietin,_and_Blood.1.aspx Kearns, C. F., & Mckeever, K. H. (2002). Clenbuterol diminishes aerobic performance in horses. Medicine & Science in Sports & Exercise, 34(12), 1976-1985. Recuperado de http://journals.lww.com/acsm-msse/Fulltext/2002/12000/Clenbuterol_diminishes_aerobic_performance_in.18.aspx Kearns, C. F., McKeever, K. H., Malinowski, K., Struck, M. B., & Abe, T. (2001). Chronic administration of therapeutic levels of clenbuterol acts as a repartitioning agent. Journal of Applied Physiology, 91(5), 2064-2070. Recuperado de http://jap.physiology.org/content/91/5/2064.full.pdf+html Kenney, W. L., Wilmore, J. H., & Costill, D. L. (2012). Physiology of Sport and Exercise (5ta. ed., p. 399, 405). Champaign, IL: Human Kinetics. Kicman, A. T. (2010). Biochemical and physiological aspects of endogenous androgens. En E. Thieme, & P. Hemmersbach (Eds), Handbook of Experimental Pharmacology 195: Doping in Sports (pp. 25-64). New York: Springer-Verlag Berlin Heidelberg. Recuperado de http://www.anabolicsteroidcalculator.com/resources/articles/ebooks/doping/chapter2.pdf Kicman, A. T., & Gower, D. B. (2003). Anabolic steroids in sport: biochemical, clinical and analytical perspectives. Annals of Clinical Biochemistry, 40(4), 321-356 Kindermann, W. (2007). Do inhaled beta(2)-agonists have an ergogenic potential in non-asthmatic competitive athletes?. Sports Medicine, 37(2), 95-102. Recuperado de la base de datos de EBSCOhost (SPORTDiscus with Full Text). Kishner, S., & Griffing, G. T. (2011). Anabolic steroid use and abuse. Medscape Reference: Drugs, Disease & Procedures. Recuperado de http://emedicine.medscape.com/article/128655-overview#a1 Kraemer, W. J., Fleck, S. J. & Deschenes, M. R. (2012). Exercise Physiology Integrating Theory and Application (p. 416, 422). Philadelphia: Lippincott Williams & Wilkins. Kuhn, C., Swartzwelder, S., & Wilson, W. (2003). Anabolizantes, estimulantes y calmantes en la práctica deportiva : información fidedigna sobre medicamentos, suplementos y entrenamiento dirigida a los deportistas (pp. 101-102). Badalona, España: Editorial Paidotribo. Recuperado de la base de datos de EBSCOhost (eBbook Collection). Kuipers, H. (1998). Anabolic
steroids: Side effects. En T. D. Fahey Leone, J. E., & Becker, L. (2008). Anabolic-Androgenic Steroids: What Teachers, Physical Educators, and Health Educators Are Talking About. Illinois Journal For Health, Physical Education, Recreation & Dance, 61, 5-13.. Recuperado de la base de datos de EBSCOhost (SPORTDiscus with Full Text). Lippi, G, Franchini, M, Salvagno, G. L, & Guidi, G. C. (2006). Biochemistry,
physiology and complications of blood doping: facts and Speculation.
Critical Reviews in Clinical Laboratory Sciences, 43(4):349–391.
Recuperado de
http://hunterp.disted.camosun.bc.ca/Blood doping paper.pdf Marban-Arcos, E., & López-Jiménez, F. (2011). Intoxicación alimentaria por clenbuterol. Revista De Sanidad Militar, 65(3), 121-124. Recuperado de la base de datos de EBSCOhost (MedicLatina). Max, S. R., & Rance, N. E. (1984). No effects of sex steroids on compensatory muscle hypertrophy. Journal of Applied Physiology, 56(6),1589-1593 McArdle, W. D., Katch, F. I., & Katch, V. I. (2013). Sports and Exercise Nutrition (4ta. ed., pp. 353-354). Philadelphia: Lippincott Williams & Wilkins. McArdle, W. D., Katch, F. I., & Katch, V. I. (2010). Exercise Physiology: Nutrition, Energy, and Human Performance (7ma. ed., pp. 538-543, 545-546, 566). Philadelphia: Lippincott Williams & Wilkins. Müller, R. K. (2010). History of doping and doping control. En E. Thieme, & P. Hemmersbach (Eds), Handbook of Experimental Pharmacology 195: Doping in Sports (pp. 1-23). New York: Springer-Verlag Berlin Heidelberg. Recuperado de http://www.anabolicsteroidcalculator.com/resources/articles/ebooks/doping/chapter1.pdf Murphy, R. J., Béliveau, L., Seburn, K. L., & Gardiner, P. F. (1996). Clenbuterol has a greater influence on untrained than on previously trained skeletal muscle in rats [Abstract]. European Journal Applied Physiology and Occupational Physiology, 73(3-4), 304-310. Recuperado de http://www.ncbi.nlm.nih.gov/pubmed/8781861 National Center for Biotechnology Information [NCBI], U.S. National Library of Medicine [NLM]. (2012). IGF1 insulin-like growth factor 1 (somatomedin C) [Homo sapiens] . Recuperado de http://www.ncbi.nlm.nih.gov/gene/3479?report=full_report National Institute of Drug Abuse [NIDA] (2012). DrugFacts: Anabolic Steroids. Recuperado de http://www.drugabuse.gov/sites/default/files/drugfactssteroids.pdf National Strength and Conditioning
Association [NSCA] (2006). Steroids: Special report. NSCA's Performance
Training Journal. Recuperado de
http://www.nsca-lift.org/WorkArea/DownloadAsset.aspx?id=3417 Panse, B. L., Arlettaz, A., Portier, H Lecoq, A-M., Ceaurriz, J D., & Collomp, K (2006). Short term salbutamol ingestion and supramaximal exercise in healthy women. British Jpurnal of Sports, Medicine, 40(7), 627-631. Recuperado de http://pubmedcentralcanada.ca/pmcc/articles/PMC2564312/pdf/627.pdf Powers, K., & Howley, E. T. (2007). Exercise Physiology: Theory and Applications to Fitness and Performance (6ta. ed., p.523). New York: The McGraw-Hill Companies, Inc. Prather, I. D., Brown, D. E, North, P., & Wilson JR. (1995). Clenbuterol: a substitute for anabolic steroids? Medicine and Science in Sports, 27(8), 1118-1121. Recuperado de http://journals.lww.com/acsm-msse/Abstract/1995/08000/Clenbuterol__a_substitute_for_anabolic_steroids_.3.aspx Reichel, C., & Gmeiner, G. (2010). Erythropoietin and analogs. En E. Thieme, & P. Hemmersbach (Eds.), Handbook of Experimental Pharmacology 195: Doping in Sports (pp. 251-294). New York: Springer-Verlag Berlin Heidelberg. Recuperado de http://www.anabolicsteroidcalculator.com/resources/articles/ebooks/doping/chapter12.pdf Rowland, T. W. (1996). Developmental Exercise Physiology (pp. 9-10). Champaign, IL: Human Kinetics. Rogozkin, V. (1979). Metabolic effects of anabolic steroids on muscle. Medicine and Science in Sports, 11(2),160-163. Recuperado de http://journals.lww.com/acsm-msse/Abstract/1979/01120/Metabolic_effects_of_anabolic_steroid_on_skeletal.7.aspx Sari, I. (2010). Anabolic androgenic steroids and dependence. Journal of Physical Education & Sport/Citius Altius Fortius, 28(4), 68-74. Recuperado de la base de datos de EBSCOhost (SPORTDiscus with Full Text). Sawka, M. N., Joyner, M. J., Miles, D. S., Robertson, R. J., Spriet, L. L, & Young, A. J. (1996). American College of Sports Medicine position stand. The use of blood doping as an ergogenic aid. Medicine & Science in Sports & Exercise, 28(10), 127-134. Recuperado de http://journals.lww.com/acsm-msse/Fulltext/1996/10000/ACSM_Position_Stand__The_Use_of_Blood_Doping_as_an.48.aspx Signorile, J. F., Kaplan, T. A., Applegate, B., & Perry, A. C. (1992). Effects of acute inhalation of the bronchodilator, albuterol, on power output. Medicine & Science in Sports & Exercise, 24(6):638-642. Sillivent, J., Blevins, J., & Peak, K. (2012). Energy Drinks: Ergolytic or Ergogenic?. International Journal of Exercise Science, 5(3), 214-222. Recuperado de la base de datos de EBSCOhost (SPORTDiscus with Full Text). Sleeper, M. M., Kearns, C. F., & Mckeever, K. H. (2002). Chronic clenbuterol administration negatively alters cardiac function. Medicine & Science in Sports & Exercise, 34(4), 643-650. Recuperado de http://journals.lww.com/acsm-msse/Fulltext/2002/04000/Chronic_clenbuterol_administration_negatively.13.aspx South African Institute of Drug Free Sport [SAIDS] (2011). Position Statement of the South African Institute of Drug Free Sport (SAIDS) on the use of supplements in sport in school-going YOUTH. Recuperado de http://www.sasma.org.za/articles/SAIDS%20Position%20Statement%20for%20YOUTH.pdf Swaminathan, R. R. (2011). Handbook of Clinical Biochemistry (2da. ed., p. 529). London: World Scientific Publishing Co. Pte. Ltd. Recuperado de la base de datos de EBSCOhost (eBbook Collection). Titchennal, C. A. (2010). Chapter 15: Ergogenic aids. En M. A. Clark & S. C. Lucett (Eds.), NASM's Essentials of Sports Performance Training (pp. 415-428). Philadelphia: Lippincott Williams & Wilkins. Underwood, L. E., & Van Wyk, J. J. (1989). Crecimiento normal y patológico. En J. D. Wilson, &D. W. Fosted (Eds.), Williams Endocrinología (7ma. ed., pp. 243-314). Argentina, Buenos Aires: Etidorial Médica Panamericana S. A. Vanberg, P., & Atar, D. (2010). Androgenic anabolic steroid abuse and the cardiovascular system. En E. Thieme, & P. Hemmersbach (Eds.), Handbook of Experimental Pharmacology 195: Doping in Sports (pp. 411-457). New York: Springer-Verlag Berlin Heidelberg. Recuperado de http://www.anabolicsteroidcalculator.com/resources/articles/ebooks/doping/chapter18.pdf Wadler, G. I., & Hainline, B. (1989). Drugs and the Athlete (pp. 58, 70). Philadelphia: F. A. Davis Company. Warpeha, J. M. (2006). Side effects of steroids. NSCA's Performance Training Journal, 15-19. Recuperado de http://www.nsca-lift.org/WorkArea/DownloadAsset.aspx?id=3417 Weiss, R. D. (2012). Drug abuse and dependence. En L. Goldman, & A. I. Schaver (Eds.), Goldman's Cecil Medicine (24th ed., p. 158). Philadelphia, PA: Elsevier, Saunders. Williams, M. H. (1998). The Ergogenics Edge: Pushing the Limits of Sports Performance (pp. 141-143). Champaign, IL: Human Kinetics. Wood, R. I. (2008). Anabolic-androgenic streroid dependence? Insights from animal an humans. Neuroendocrinology, 29(4), 490-506. Recuperado de http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2585375/ Wolfarth, B., Wuestenfeld, J. C., & Kindermann, W. (2010). Ergogenic effects of inhaled ß2-Agonists in non-asthmatic athletes. Endocrinology and Metabolism Clinics of North America, 39(1), 75-87. Recuperado de http://webdoc.nyumc.org/nyulmc-rehab/files/nyulmc-rehab/u19/B2_Agonists_and_performance_.pdf Zeman, R. J., Zhang, Y., & Etlinger, J. D. (1994). Clenbuterol, a beta 2-agonist, retards wasting and loss of contractility in irradiated dystrophic mdx muscle. American Journal of Physiology, 267(3 Pt 1), C865-C868.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||